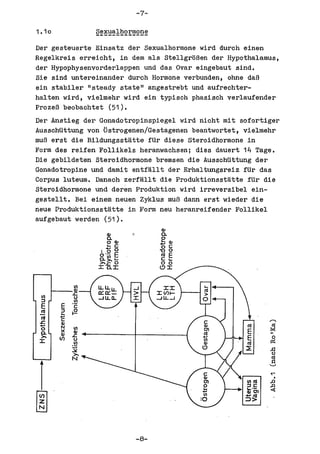
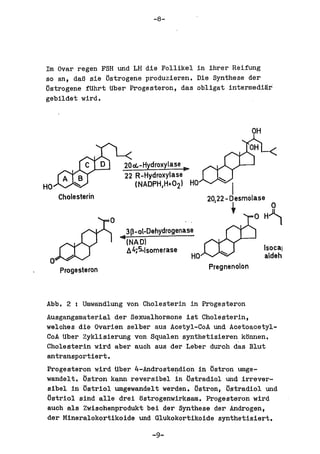
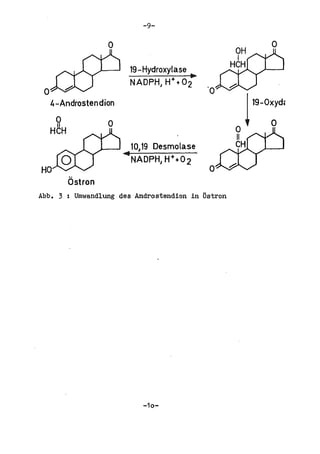
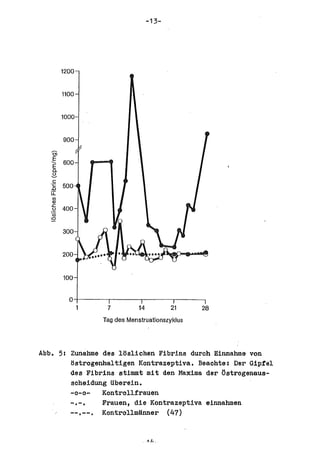
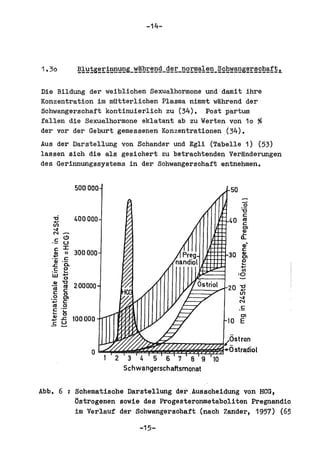
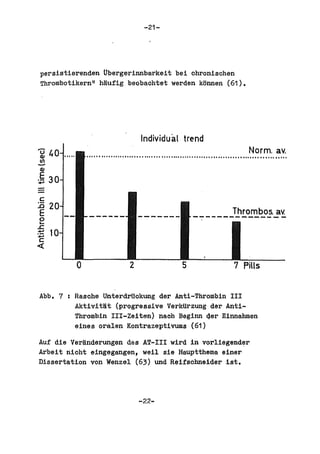
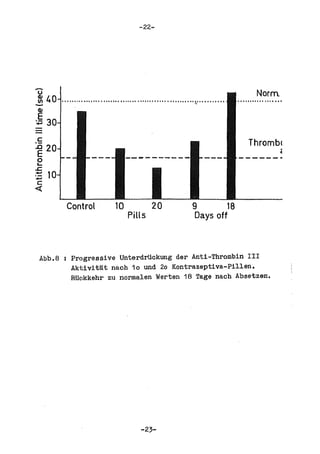
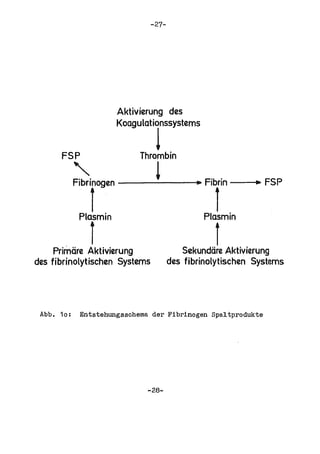
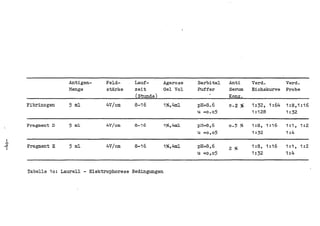
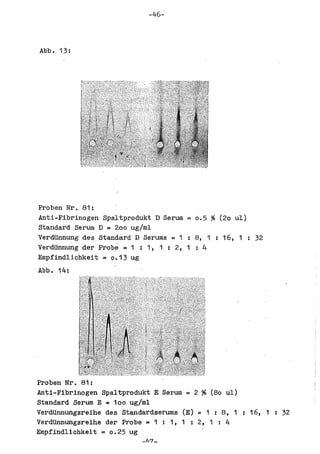
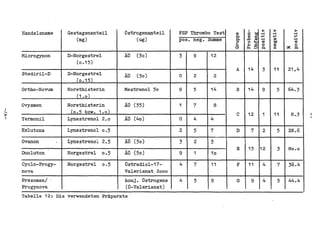
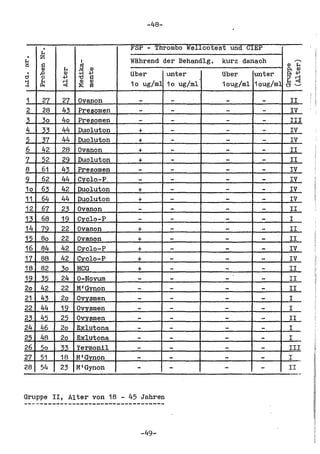
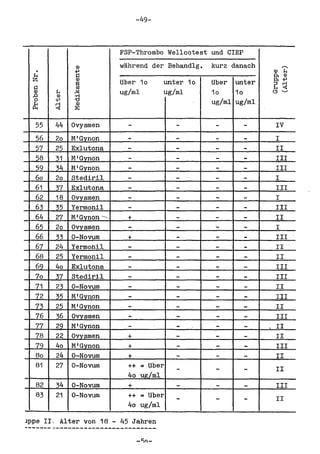
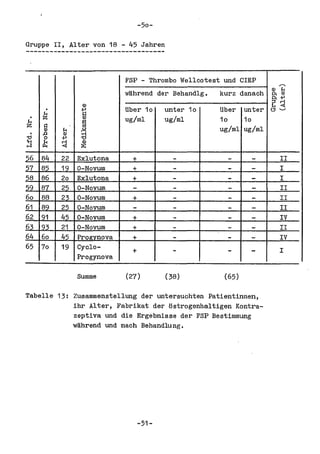
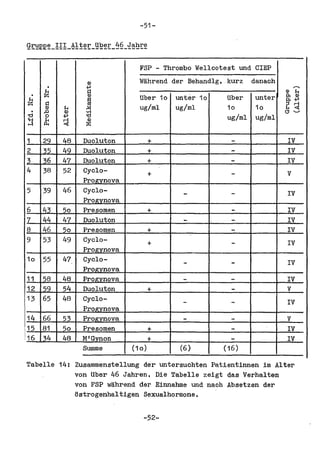
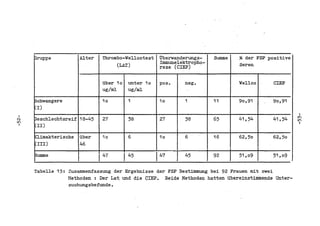
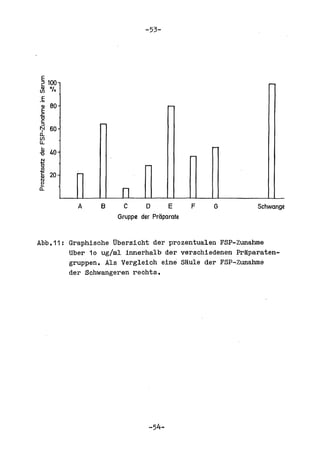
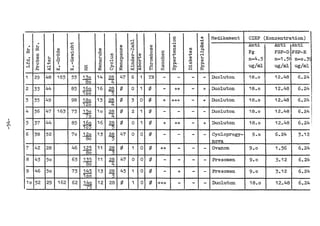
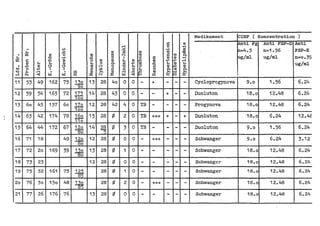
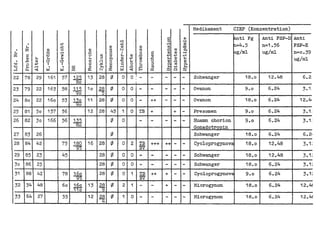
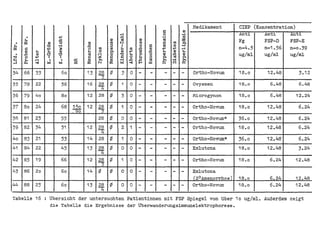
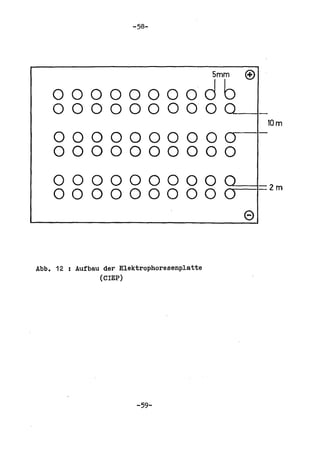
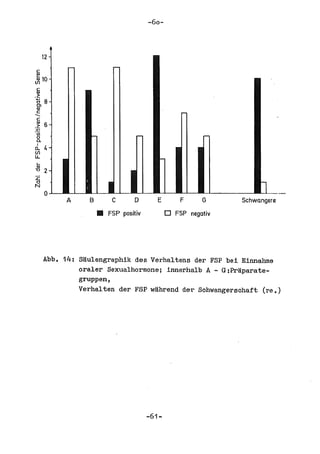
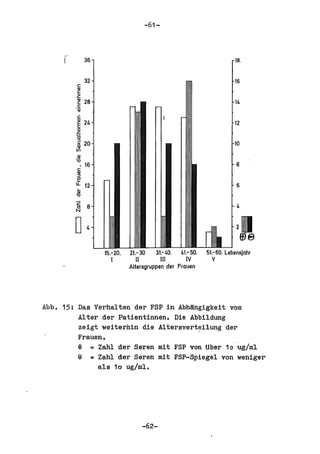
Die Dissertation von Edwin Oseni-Momonu untersucht den Nachweis von Fibrinogen- und Fibrinspaltprodukten bei Frauen, die Sexualhormone einnehmen, und deren Bedeutung für die Thromboseentstehung. Es wird festgestellt, dass die Einnahme von weiblichen Sexualhormonen das Gerinnungssystem beeinflusst und zu Veränderungen der Fibrinogenwerte führt, was pathologisch sein kann. Die Ergebnisse basieren auf verschiedenen Untersuchungsmethoden und zeigen, dass erhöhte Spiegel von Fibrinspaltprodukten mit thrombotischen Komplikationen korrelieren können.