Patologia masculina
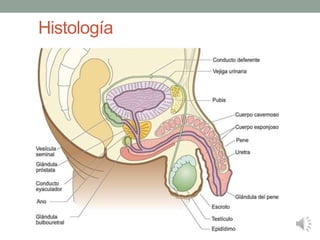
- 1. Histología
- 4. Pene: patología 1. Malformaciones congénitas: Epispadias: se asocia a otros defectos como la criptorquidia. Son causas de esterilidad. Hipospadias: mas frecuente (1/300)
- 5. Fimosis: - Puede ser una anomalía del desarrollo o por infecciones repetidas. - Es un prepucio muy pequeño que impide su retracción. - Interfiere con la higiene por el acumulo de secreciones, que puede causar infecciones y probable carcinoma.
- 6. 2. Inflamaciones: Inflamación del glande y prepucio. Infecciones específicas: Son ETS, sífilis, gonorrea, chancroide (HD), granuloma inguinal, linfogranuloma venéreo (KG) y herpes genital (VHS-2). Infecciones inespecíficas: “Balanopostitis” causado por cándida albicans, bacterias anaerobias, gardnerella y bacterias piógenas. Se presenta por mala higiene, acumulación de esmegma.
- 7. Tumores benignos del pene a) Condiloma acuminado • Común en jóvenes sexualmente activos con predilección para zonas anogenitales. • Glande > prepucio > uretra distal > cuerpo. • VPH 6 y 11, otros tipos 16, 18, 30 a 32, 42 a 44 y 51 a 55. • Macro: mayoría lesiones verrucosas y papilares, pero pueden ser planas • Mayoría son benignos, pero pueden transformarse. • Aumenta el riesgo para cáncer Anogenital. • Lesiones pequeñas son tratadas con crioterapia, electrocoagulación y ablación laser; mediano a grandes con cirugía.
- 8. a) Condiloma acuminado Histología: epitelio con hiperqueratosis superficial, paraqueratosis, acantosis y papilomatosis. Vacuolización citoplasmática (coilocitosis) característica de la infección por VPH.
- 9. Tumores malignos del pene A. CARCINOMA IN SITU (CIS) Asociado a VPH tipo16 (80%). 1. Enfermedad de Bowen: en varones mayores de 35 años, afecta la piel del pene y escroto. Macroscopía: placa solitaria, engrosada, blanca grisácea y opaca. En glande y prepucio placas aisladas de color rojo brillante. Histología: células epiteliales disqueratósicas y displásicas con mitosis encima de la capa basal. Membrana basal intacta. Puede transformarse en cáncer invasivo en el 10% de los casos
- 10. 2. Eritroplasia de Queyrat exclusivamente en hombres no circuncidados, ocurre en el glande en el sulcus coronal o en la superficie interna del prepucio, se manifiesta como una placa rojo-brillante, bien delimitada. 3. Papulosis bowenoide: se presenta en adultos jovenes sexualmente activos, usualmente son lesiones papulares marrón rojizo y múltiples pequeñas, en el glande o cuerpo, prepucio, escroto, piel inguinal. Nunca evoluciona a carcinoma invasivo y en muchos casos regresionan espontáneamente.
- 11. Carcinoma epidermoide del pene Epidemiología • Representa 10 a 20% en Asia, África y Sudamérica • Edad media 60 años • La circuncisión protege. • Aproximadamente un 50% están asociados a PVH tipo 16 y 18. • El consumo de cigarro incrementa el riesgo. Presentación clínica • Usualmente como lesión papilar y exofítica. • A veces lesiones planas y ulceradas • Es posible invasión en el cuerpo y la uretra, importante para manejo y pronóstico. • Metástasis inguinal ulcerada en casos avanzados
- 12. Morfología: Comienza en el glande o en la superficie interna del prepucio. Hay dos patrones macroscópicos, el papilar y el plano. Las lesiones papilares simulan condilomas acuminados como coliflor. Las lesiones planas son zonas de engrosamiento epitelial con fisuras y ulceraciones. El carcinoma verrugoso es una variante exofítica bien diferenciada de baja malignidad, raro metástasis.
- 14. Pronóstico y tratamiento • El pronóstico varia con el estadio clínico e incluye Rt, Qt y Cx • El espesor, nivel de invasión, grado de diferenciación y presencia de invasión vascular y perineural, son predictores pronósticos.
- 18. Testículo: patología • Malformaciones congénitas: • Criptorquidia • Cambios regresivos: • Atrofia y reducción de la fertilidad • Inflamación: • Epididimitis y orquitis inespecífica • Orquitis granulomatosa (autoinmunitaria). • Problemas vasculares: • Torsión
- 19. Criptorquidia • Se detecta en el 1% de los niños de 1 año de edad, representa un fracaso completo o incompleto del descenso de los testículos al escroto. • Niños a término 3%, prematuros 30%. 80% desciende en el primer año. • Mayoría unilateral, 25% bilateral. • Dos fases: -transabdominal controlada por hormona inhibidora mülleriana. -Inguinoescrotal depende de andrógenos. • Alto riesgo de esterilidad, después de 2 años. • Riesgo de 3 a 5 veces mayor de cáncer testicular. • Riesgo mayor de torsión. • Orquiopexia entre 6 a 12 meses reduce el riesgo. TIPOS
- 20. Los cambios histológicos comienzan a los 2 años y se caracterizan por detención de la espermatogénesis, hialinización y engrosamiento de la lámina basal de los túbulos seminíferos y aumento de las células de Leydig.
- 21. Cambios regresivos: 1. Atrofia y reducción de la fertilidad: Causas: 1) estenosis aterosclerótica progresiva, 2) orquitis terminal, 3) criptorquidia, 4) hipopituitarismo, 5) malnutrición y caquexia, 6) irradiación, 7) administración prolongada de antiandrógenos, y 8) atrofia por agotamiento. Los cambios macro y microscópicos son de la criptorquidia. En ocasiones, la atrofia se produce por un fracaso primario de origen genético, como el Síndrome de Klinefelter.
- 22. Inflamaciones: • Causas específicas de orcoepididimitis: TBC, gonorrea y sífilis. • Causas inespecíficas: de infecciones urinarias. En varones activos y < 35 años: C. trachomatis y n. gonorrhoeae. En > 35 años: E. coli y pseudomona.
- 23. Tumores testiculares: Clasificación 1. Tumores de Células Germinales: (95%) A. Tumores Seminomatosos: Seminoma Clásico o Típico (50%) Seminoma Espermatocítico. B. Tumores no Seminomatosos: Carcinoma Embrionario. Tumor del Saco Vitelino.(mas frecuente en lactantes y niños < 3ª, α fetoproteina positivo) Coriocarcinoma.(Gonadotrofina corionica-HCG elevado) Teratoma. 2. Tumores de los cordones sexuales y del estroma: A. Tumores de las células de Leydig. B. Tumores de las células de Sertoli.
- 24. Seminoma clásico Mas frecuente en la 3ra década. Factor de riesgo: Criptorquidia MORFOLOGÌA: Son masas voluminosas (10v). Superficie de corte homogénea blanca grisácea y lobulado sin hemorragia o necrosis. Es bien delimitado y no atraviesa la túnica albugínea. Son radiosensibles.
- 25. SEMINOMA CLÁSICO Microscópicamente, el Seminoma típico esta formado por sábanas de células uniformes divididos en lóbulos mal delimitados por tabique de tejido conectivo con linfocitos. Se parece al disgerminoma.
- 26. La célula clásica del seminoma es grande y redonda o poliédrica y tiene una membrana celular diferenciada, un citoplasma claro que contiene glucogeno y un gran núcleo central pálido con 1 o 2 nucléolos prominentes. Las mitosis son variables. SEMINOMA CLÁSICO
- 27. Seminoma espermatocítico Es un tumor infrecuente (1-2%). Edad > a 65 años. Crecimiento lento y sin metástasis. Morfología: macroscopicamente al corte superficie blanda y gris clara. Histología: tres poblaciones celulares entremezcladas, 1) células de mediano tamaño, las más numerosas, con núcleos redondos y citoplasma eosinófilo; 2) otras células mas pequeñas parecido a espermatocitos secundarios y 3) células gigantes uni o multinucleadas. Carecen de linfocitos.
- 28. Carcinoma embrionario Edad 20 a 30 años. Mas agresivos que los seminomas. Morfología: son mas pequeños que el seminoma, aspecto variado, mal delimitado, con hemorragia y necrosis. Es frecuente la extensión a través de la túnica albugínea hacia el epidídimo.
- 29. Carcinoma embrionario Histología: las células crecen adoptando patrones alveolares o tubulares y a veces papilares. Las lesiones mas indiferenciadas pueden mostrar sábanas de células. Las células tienen aspecto epitelial, son grandes y anaplásicas con núcleos hipercromáticos y nucléolos prominentes.
- 30. Teratoma Tumores testiculares complejos que tienen varios componentes celulares u organoides procedentes de mas de una capa germinal. Se presentan a cualquier edad. Macro: 5 a 10 cm, heterogéneo con zonas sólidas, cartilaginosas y quísticas.
- 31. Teratoma Micro: Tejido neural, haces musculares, islotes de cartílago, grupos de epitelio escamoso, glándulas tiroides, epitelio bronquial; todo en un estroma fibroso o mixoide.
- 32. Tumor del Seno Endodermico Es el tumor mas frecuente en lactantes y niños de hasta 3 años. Morfología: no están encapsulados y presentan un aspecto mucinoso homogéneo, amarillo o blanco. Histologicamente están compuestos por una red reticular de células cúbicas y aplanadas . Además puede haber estructuras papilares, cordones solidos. Aproximadamente en el 50% puede verse estructuras que parecen senos endodermicos (cuerpos de Schiller-Duval), que tienen un aspecto glomeruloide. Dentro y fuera del citoplasma se observan glóbulos hialinos eosinófilos que contienen α-fetoproteina (AFP).
- 33. Coriocarcinoma Es el tumor mas maligno, en su forma pura son raros, menos del 1%. Morfología: No causan aumento del tamaño testicular, son sólo nódulos pequeños periféricos menos de 5 cm. Son frecuentes las hemorragias y necrosis. Histológicamente contienen dos tipos de células, sincitiotrofoblastos son células grandes multinucleadas con abundante citoplasma eosinofilo vacuolado que contiene HCG y citotrofoblastos son mas regulares y poligonales , bordes delimitados , citoplasma transparente y un solo núcleo. Pueden formar cordones o masas celulares.
- 34. Próstata histología Próstata macro Próstata micro
- 38. Próstata: patología La prostatitis se divide en: prostatitis bacterianas agudas y crónicas, prostatitis abacteriana crónica y prostatitis granulomatosa. La prostatitis bacteriana aguda es por E. coli, otros gram negativos, enterococos y estafilococos. Vía urinaria, hematógena o local. La prostatitis bacteriana crónica por infecciones repetidas de las vías urinarias. La prostatitis abacteriana crónica es la forma mas frecuente, no hay antecedentes de ITU, hay > 10 leucocitos en la secreción prostática con cultivo ( - ). La prostatitis granulomatosa pueden ser especificas y inespecificas. BCG, micóticas, reacción a secreciones ( mas frecuente). Contraindicado la biopsia prostática por riesgo de sepsis. Inflamación
- 39. Hiperplasia prostática benigna (HPB) Hiperplasia glandular y estromal, en la región periuretral de la próstata. Se inicia en los 40 años en 20% de los varones. Patogenia: Aunque la causa de la HPB es desconocida, se cree que los factores de crecimiento (FGB, TGF-β) inducidos por DHT actúan aumentando la proliferación de las células estromales y disminuyendo la muerte de las células epiteliales.
- 40. Se originan de la zona interna de la glándula. Los nódulos iníciales están formados casi exclusivamente por células estromales y luego aumentan las células epiteliales. Por su origen casi siempre comprime a la uretra. Al corte el color y la consistencia varia si son a predominio glandular o estromal, de un color rosado o amarillo a un gris claro de consistencia fibrosa. Patología
- 42. Microscópicamente, la característica de la HPB es la nodularidad. Los nódulos varían de fibromusculares puramente a nódulos fibroepiteliales con predominio glandular. La proliferación glandular adopta la forma de agregados de glándulas pequeñas a grandes o con dilataciones quísticas recubiertas por dos capas, una cilíndrica interna y un epitelio cúbico o aplanado exterior. Patología
- 43. Adenocarcinoma de próstata Epidemiología • Tercera causa de muerte en países en vías de desarrollo. • Múltiples factores genéticos y ambientales. • Edad, historia familiar y raza son factores de riesgo. • Raza negra tiene mayor incidencia, mayor grado y mayor estadio. • Dieta rica en grasa y niveles de hormonas son probables factores de riesgo. • Los andrógenos tienen un papel importante en el desarrollo del cáncer de próstata. • Antecedente de familiar de 1er grado con cáncer. • Variaciones en la mutación del gen supresor BRCA 2, locus de riesgo en q24, reordenamiento cromosómico del ETS (ERG o ETV1) al gen TMPRSS2 regulado por andrógenos.
- 45. Factores de Riesgo • ESTABLECIDOS: Origen étnico. • EDAD, historia familiar, dieta. • POSIBLE: lycopene, zinc, selenium. • INCIERTO: polimorfismo en R.A. y Vitamina D. • EXCLUIDOS: fumar, alcohol, vasectomía y actividad física.
- 46. Neoplasia Intraepitelial Prostática (PIN): Lesión precursora
- 47. PIN DE ALTO GRADO • Definición: acino prostático arquitecturalmente benigno y ducto tapizado por células atípicas. • Incidencia: rango de 0 – 24.6%, media 7.7 % y mediana 5.2%. • Reproducibilidad interobservador: diagnóstico subjetivo (alta en uropatólogos, moderada en otros). • Marcador inmunohistoqumico: α-metilacil- coenzima A-racemasa (AMACR) positivo en cancer con una sensibildad 80% - 100%.
- 48. PIN DE ALTO GRADO
- 49. • Riesgo de cáncer: 31.5 % (mediana 24.1%). • Riesgo de cáncer estratificado por predictores clínicos: No hay parámetro clínico que ayude. • Riesgo estratificado por número de cores: hay reportes que > 2 cores con PINHG, el riesgo en la re biopsia es 58%, contra 16% <o= 2 cores. • Riesgo y patrón morfológico: Plano/tufted<micropapilar/cribiforme PIN DE ALTO GRADO
- 50. Presentación clínica • Mayoría son asintomáticos. • El 70% se originan en la zona periférica. • Puede comprometer la vejiga y el recto y causar hematuria y sangrado rectal u obstrucción. • Raramente exhiben síntomas de la metástasis, comúnmente hueso (lesión osteoblastica), ganglios linfáticos, pulmón y cerebro
- 51. PSA • Glucoproteína • Peso: 35.000 daltons • Es específico del órgano, pero no tan específico del cáncer. • Elevación: Cáncer de próstata 25% - 90% Valor > 4 ng/dl Sensibilidad 79% • Benignas: Prostatitis, HPB 30% - 50% Eyaculación, biopsia, ecografía TR 51
- 52. 52 PSA • Útil tamizaje: TR y Ecografía • Niveles según: Edad, Velocidad elevación, PSA libre Velocidad 0,75 ng/ml por año PSA libre < 10% Índice PSA libre / PSA total < 11% • Postquirúrgico: 14 días • Útil en seguimiento • Cada 6 meses por 5 años
- 53. 53 EDAD (años) LÍMITE SUPERIOR NORMAL (ng/dl) < 40 < 3,5 40 – 49 < 3,8 50 – 59 < 4,0 60 – 69 < 5,4 70 – 79 < 6,3 ≥ 80 < 6,6
- 54. Tipo Histológico • Acinar • Ductal • Mucinoso • Céls. en anillo de sello • Adenoescamoso • Basaloide y adenoide quístico • Urotelial • Células pequeñas • Otros
- 55. PATOLOGÍA Frecuentemente es la variante acinar del cáncer de próstata. El 70% de los casos surgen de la zona periférica de la glándula y de localización posterior. Al corte el tejido neoplásico es arenoso y firme.
- 56. PATOLOGÍA Histológicamente , la mayoría son adenocarcinomas que producen un patrones glandulares bien definidos. Son mas pequeñas que las normales y están revestidas por una sola capa de células cúbicas o cilíndricas bajas. La capa externa de células basales está ausente. Al contrario de lo que sucede en las glándulas benignas, las glándulas del cáncer de próstata están mas apiladas y carecen de ramificaciones.
- 57. PATOLOGÍA
- 59. CLASIFICACIÓN DE GLEASON Clasificación de Gleason: Grado 1: bien diferenciado (glándulas) Grado 5: indiferenciado ( cordones y laminas de células malignas) Puntuación o graduación: 1+1=2……….5+5=10. Puntuación 2- 4: cáncer bien diferenciado. 5 – 6: grado intermedio. 7: indiferenciado. 8 – 10 : cáncer avanzado de alto grado.
- 60. E. Gleason / grado histológico Escore Gleason Bien diferenciado 2 - 6 Moderadamente diferenciado 7 Pobremente diferenciado 8 – 10
- 61. Estadificación sistema TNM TNM Resultado T1 Lesión clínicamente no evidente T2 Cáncer palpable o visible confinado a la próstata T3 Extensión local extra prostática T4 Invasión de órganos contiguos, N0 Sin metástasis en ganglios N1 Metástasis en ganglios regionales M0 Sin metástasis a distancia M1 Metástasis a distancia presente
- 62. Pronóstico y tratamiento • El tratamiento depende del estadio y grado del tumor • La prostatectomia radical, localmente avanzado combinación de Radioterapia y Hormonoterapia de ablación. • Pronóstico depende del huésped, tumor y parámetros del tratamiento
- 63. GRACIAS
- 64. Fuentes de información • Fuentes bibliográficas: • ROBBINS Y COTRAN. PATOLOGÍA ESTRUCTURAL Y FUNCIONAL; 9ra Edición. Ed. Elsevier, año 2015. • RUBIN’S PATHOLOGY Clinicopathologic Foundations of Medicine; sixth edition, Editorial Lippincott Williams and Wilkins. Philadelphia 2012
Hinweis der Redaktion
- Documento para planeación 2002-2003
- Documento para planeación 2002-2003
- Documento para planeación 2002-2003
