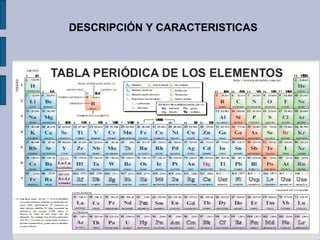
Primer trimestre química I
- 2. Antecedente D.I. Mendeleiev en 1869, agrupo los elementos químicos en una tabla con base a su MASA ATOMICA.
- 3. Características FAMILIAS / GRUPOS constan de 18 columnas verticales. Se nombran desde la izquierda a la derecha por números romanos y una letra A o B. También se designan con los números del 1 al 18
- 4. Características GRUPO representativo «A» IA ALCALINOS IIA ALCALINOS TERREOS IIIA BOROIDES IVA CARBONOIDES VA NITROGENOIDES VIA CALCOGENOS ó Anfígenos VIIA HALOGENOS VIIIA GASES NOBLES
- 5. Características GRUPO transición «B» IIIB FAMILIA SCANIO IVB FAMILIA TITANIO VB FAMILIA VANADIO VIB FAMILIA CROMO VIIB FAMILIA MANGANESO VIIIB FAMILIA HIERRO VIIIB FAMILIA COBALTO VIIIB FAMILIA NIQUEL IB FAMILIA COBRE IIB FAMILIA ZINC
- 6. Características PERIODOS Son siete filas horizontales señaladas con números arábigos ( 1; 2; 3, 4 ; 5; 6; 7) . Los tres primeros son periodos cortos y los siguientes son largos.
- 9. Características Elementos de transición interna.
- 10. Características Diagrama de la tabla periódica según orbitalesDiagrama de la tabla periódica según orbitales
- 11. Propiedades Periódicas Relaciones de Tamaño Relaciones de Energía Radio atómico Radio iónico Potencial de ionización Electroafinidad Electronegatividad Carácter del elemento Propiedades PeriódicasPropiedades Periódicas de los Elementosde los Elementos
- 12. Enlaces y Reacciones: 11 Cuando los átomos entran en interacción mutua, de modo que se completan sus niveles energéticos exteriores, se forman partículas nuevas más grandes. 22 Estas partículas constituidas por dos o más átomos se conocen como moléculas y las fuerzas que las mantienen unidas se conocen como enlaces.
- 13. Tipos de Enlaces Hay dos tipos principales de enlaces: iónico y covalente. Los enlaces iónicos se forman por la atracción mutua de partículas de carga eléctrica opuesta; esas partículas, formadas cuando un electrón salta de un átomo a otro, se conocen como iones Para muchos átomos, la manera más simple de completar el nivel energético exterior consiste en ganar o bien perder uno o dos electrones. (enlace entre un metal y un no metal)
- 15. Tipos de Enlaces EnlaceEnlace IónicoIónico Un enlace iónico es la fuerza de la atracción electrostática entre iones de carga opuesta. ClCl–– (anión)(anión))) KK++ ((catióncatión))
- 16. Tipos de Enlaces Los enlaces covalente están formados por pares de electrones compartidos. Un átomo puede completar su nivel de energía exterior compartiendo electrones con otro átomo. En los enlaces covalentes, el par de electrones compartidos forma un orbital nuevo (llamado orbital molecular) que envuelve a los núcleos de ambos átomos.
- 17. Tipos de Enlaces :: FF :: .... .... CC :: FF :: .... .... :: FF :: .... ....:: FF :: .... .... comocomo CCFF FF FF FF .... .... .... ....:: :: :: :: :: :: ....
- 18. FuerzasFuerzas intermolecularesintermoleculares Las fuerzas intermoleculares son fuerzas electromagnéticas las cuales actúan entre moléculas o entre regiones ampliamente distantes de una macromolécula. Fuerzas de los Enlaces
- 19. Fuerzas IntermolecularesFuerzas IntermolecularesFuerzas IntermolecularesFuerzas Intermoleculares Fuerzas electromagnéticas Dipolo-Dipolo- dipolodipolo DispersiónDispersión PuentePuente hidrhidrógenoógeno
- 20. Dipolo-Dipolo Son las fuerzas que ocurren entre dos moléculas con dipolos permanentes. Estas funcionan de forma similar a las interacciones iónicas, pero son más débiles debido a que poseen solamente cargas parciales. Un ejemplo de esto puede ser visto en el acido clorhídrico: (+)(-) (+)(-) H-Cl----H-Cl (-)(+) (-)(+) Cl-H----Cl-H
- 21. Dispersión Son pequeñas y transitorias fuerzas de atracción entre moléculas no polares. Son más intensas en las moléculas no polares más grandes que en las pequeñas. Son de mayor magnitud en el Br2, que en el I2, que en el F2.
- 22. Puente de hidrógeno Es un tipo de atracción dipolar particularmente fuerte, en el cual un átomo de hidrógeno hace de puente entre dos átomos electronegativos, sujetando a uno con un enlace covalente y al otro con fuerzas puramente electrostáticas.