Simulado b iii
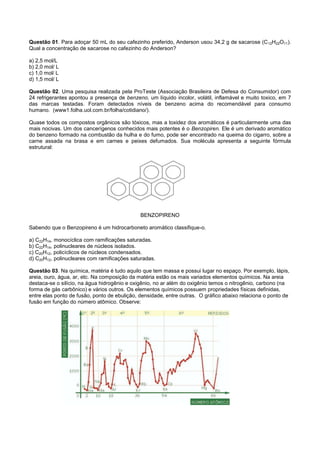
- 1. Questão 01. Para adoçar 50 mL do seu cafezinho preferido, Anderson usou 34,2 g de sacarose (C 12H22O11). Qual a concentração de sacarose no cafezinho do Anderson? a) 2,5 mol/L b) 2,0 mol/ L c) 1,0 mol/ L d) 1,5 mol/ L Questão 02. Uma pesquisa realizada pela ProTeste (Associação Brasileira de Defesa do Consumidor) com 24 refrigerantes apontou a presença de benzeno, um líquido incolor, volátil, inflamável e muito toxico, em 7 das marcas testadas. Foram detectados níveis de benzeno acima do recomendável para consumo humano. (www1.folha.uol.com.br/folha/cotidiano/). Quase todos os compostos orgânicos são tóxicos, mas a toxidez dos aromáticos é particularmente uma das mais nocivas. Um dos cancerígenos conhecidos mais potentes é o Benzopiren. Ele é um derivado aromático do benzeno formado na combustão da hulha e do fumo, pode ser encontrado na queima do cigarro, sobre a carne assada na brasa e em carnes e peixes defumados. Sua molécula apresenta a seguinte fórmula estrutural: BENZOPIRENO Sabendo que o Benzopireno é um hidrocarboneto aromático classifique-o. a) C22H14, monocíclica com ramificações saturadas. b) C22H14, polinucleares de núcleos isolados. c) C20H12, policíclicos de núcleos condensados. d) C20H12, polinucleares com ramificações saturadas. Questão 03. Na química, matéria é tudo aquilo que tem massa e possui lugar no espaço. Por exemplo, lápis, areia, ouro, água, ar, etc. Na composição da matéria estão os mais variados elementos químicos. Na areia destaca-se o silício, na água hidrogênio e oxigênio, no ar além do oxigênio temos o nitrogênio, carbono (na forma de gás carbônico) e vários outros. Os elementos químicos possuem propriedades físicas definidas, entre elas ponto de fusão, ponto de ebulição, densidade, entre outras. O gráfico abaixo relaciona o ponto de fusão em função do número atômico. Observe:
- 2. De acordo com o gráfico, marque a opção INCORRETA: a) Possuem ponto de fusão inferior a 1000 °C 13 elementos químicos, sendo o Sódio o elemento com PF mais elevado. b) Dentre os elementos do 6° período, tanto o césio quanto o mercúrio, apresentam PF próximo a 0°C. c) O elemento químico cujo número atômico é 18 possui ponto de fusão >0. d) Apenas um elemento do 4° período possui PF entre 2000 e 3000 °C. Questão 04. A aspirina é um medicamento proveniente de uma planta bastante popular, o salgueiro. É utilizada como anti-inflamatório e analgésico. Seu princípio ativo consiste no ácido acetilsalicílico conhecido como AAS ou apenas AS. É um ácido fraco, pouco solúvel em água. Apresenta ponto de fusão igual á 135°C e ponto de ebulição 140°C. Observe abaixo sua estrutura molecular: Sobre a molécula acima foram realizadas as seguintes afirmações: I- Composto orgânico com formula molecular C9H8O4 e pH inferior a 7. II- Composto inorgânico, com massa molecular igual a 180 g/mol. III- Em temperaturas entre 135 e 140°C encontra-se no estado líquido, apresenta pH inferior a 7 e massa molecular igual a 180 g/mol. IV- Composto orgânico com formula molecular igual a C9H8O4, em temperatura ambiente encontra-se no estado sólido. Dados: C= 12g/mol; H=1g/mol; O=16g/mol. Estão corretas apenas: a) apenas I b) I e III c) II e IV d) III e IV Questão 05. Um dos produtos usados na construção civil é a areia, que precisa ser de boa qualidade, porém quando ela é recolhida pelas dragas, um grande número de impurezas também é coletado: pedaços de madeiras, fragmentos de rochas e outros. Para separar a areia desses materiais, qual técnica a seguir é mais bem empregada? a) Decantação b) Filtração c) Peneiração d) Sedimentação Questão 06. A morfina é um fármaco nárcotico do grupo dos opoídes, que é usada no tratamento sintomático da dor. Analise sua estrutura e responda quantos carbonos primários tem nessa estrutura:
- 3. a) 3 carbonos primários b) 2 carbonos primários c) 1 carbono primário d) 4 carbonos primários Questão 07. Foi observado que o cozimento de meio quilo de batata em 1litro de água (H 2O) é mais rápido se adicionar 200 gramas de sal de cozinha (NaCl) à água de cozimento. Considere as seguintes possivéis explicações para o fato: I. A adição de sal provoca um aumento da temperatura de ebulição da água; II. A adição de sal provoca um aumento da pressão de vapor da água; III. O sal adicionado não altera a temperatura de ebulição da água, mas reage com o amido da batata. Dentre essas alternativas qual esta correta: a) Apenas I b) Apenas II e III c) Apenas I e II d) Apenas I II e III Questão 08. A sabedoria popular indica que, para acender uma lareira, devemos utilizar inicialmente lascas de lenha e só depois colocarmos as toras. Em condições reacionais idênticas e utilizando massas iguais de madeira em lascas e em toras, verifica-se que madeira em lascas queima com mais velocidade. O fator determinante, para essa maior velocidade da reação, é o aumento da: a) Pressão b) Temperatura c) Concentração d) Superfície de contato Questão 09. O ácido clorídrico e muito usando industrialmente na manufatura de corantes. Com o nome de ácido muriático ele é largamente empregado na limpeza em geral, não podendo ser utilizado, no entanto, em pisos de mármore, os quais são constituídos de carbonato de cálcio. Se por acidente um pouco de ácido muriático cair sobre o piso de mármore, entre os produtos citados abaixo, normalmente encontrados em qualquer residência, o mais indicado para se espalhar e sobre local será: a) Vinagre b) Suco de Limão c) Sal de Cozinha d) Amoníaco Questão 10. No café da manhã ou no lanche da tarde, muitas vezes em casa, temos um delicioso bolo feito por nossas mães ou avós, que de tão fofinho, desmancha na boca. Isso ocorre pela presença do bicarbonato de sódio (NaHCO3) no fermento químico. Ao ser aquecido, o NaHCO3 libera dióxido de carbono (CO2), que faz com que a massa do bolo cresça e fique aerada. Podemos ver isso pela reação, não balanceada, abaixo: NaHCO3 → Na2CO3 + H2O + CO2 Para balancear esta reação, qual deve ser, respectivamente, o número de mols de NaHCO 3, Na2CO3 , H2O e CO2 ? a) 2;1;1;1; b) 1;2;1;1;
- 4. c) 1;1;2;1; d) 1;1;1;2. Questão 11. Os desagradáveis odores de transpiração são provocados por alguns ácidos carboxílicos presentes no suor. O composto a seguir que pode ser utilizado para eliminar esse mau cheiro é: a) Açúcar (glicose) b) Sal de cozinha (cloreto de sódio) c) Vinagre (solução diluída de ácido acético) d) Leite de magnésia (hidróxido de magnésio) Questão 12. Patrícia, estudante do 1º ano do Ensino Médio, vendo sua mãe Joana preparar o jantar notou que, quando a água do arroz que contém o sal de cozinha (NaCl) escorre pela panela e atinge a chama azul do fogo, imediatamente surge uma coloração amarela bem forte. Ao questionar seu professor sobre o que causou a mudança na cor da chama ele explicou que os elétrons que giram em todo do núcleo dos átomos de alguns elementos, nesse caso o Sódio, ao absorverem energia em forma de calor, ‘saltam’ para um nível de energia maior e ao retornar para seu nível normal, liberam energia em forma de luz. Esse fenômeno pode ser explicado pelo modelo atômico proposto por: a) Niels Bohr b) John Dalton c) J. J. Thomson d) Ernest Rutherford