Manganeso
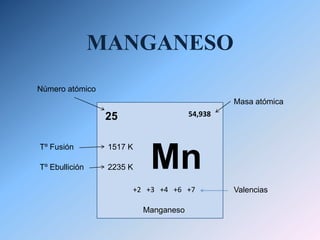
- 1. MANGANESO Número atómico Masa atómica 25 54,938 Mn 1517 K Tº Fusión 2235 K Tº Ebullición +2 +3 +4 +6 +7 Valencias Manganeso
- 4. Glauber, un químico alemán produjo permanganato por primera vez en el siglo XVII.
- 5. Más tarde fue Scheele un químico sueco que descubrió que el manganeso era un elemento.
- 6. Johann Gottlieb Gahn quien aisló el manganeso por reducción del dióxido de carbono en 1774, por esta razón se le atribuyé a él el descubrimiento de este elemento.
- 8. Tiene un color grisáceo plateado.
- 9. Su punto de fusión, es decir, la temperatura en la que el elemento pasa de estado sólido a estado líquido es de 1246 ºC.
- 10. Su punto de ebullición, temperatura a la que el elemento pasa de estado líquido a estado gaseoso es de 2061 ºC.
- 11. Su volumen atómico es de 7,35 cm3/mol.
- 12. Su masa atómica es de 54,938 g/mol.
- 13. Su dureza, resistencia al rayado. varia desde 2 (terrosos) a 5-6 (cristales)
- 15. Su radio atómico, es la distancia que hay desde el núcleo del átomo hasta la capa de valencia más externa lo que nos permite determinar el tamaño del átomo, es 1,35 Å.
- 16. Su electronegatividad, capacidad del átomo de atraer hacia él los electrones, es 1,55.
- 17. Su radio iónico, distancia que hay desde el núcleo del átomo hasta la capa de valencia más externa pero haciendo referencia al ión, es de 0,80 (+2), 0,46 (+7) Å.
- 19. En aleación con antimonio y aluminio y con pequeñas cantidades de cobre son ferromagnéticas, es decir, capacidad de producir ordenamiento magnético de los elementos magnéticos de una muestra, en la misma dirección y sentido.
- 20. Se utiliza en la fabricación de resistencias invariables con la temperatura con calcio y níquel.
- 21. El dióxido de manganeso se usa como decolorante y colorante del vidrio como hemos dicho antes, debido a la presencia de hierro, como catalizador para barnices y pinturas, como despolarizador de pilas secas, para fabricar cloro…
- 22. El permanganato de potasio lo utilizamos para decolorar aceites ya que es un fuerte agente oxidante.
- 24. Implica la correcta utilización de las vitaminas B1 y E.
- 25. Se combina con el Zinc para tratamientos de esquizofrenia.
- 26. Participa en un gran número de reacciones orgánicas.
- 27. Sintetiza la aceltilcolina para prevenir la diabetes mellitus.
- 28. Ayuda en la formación de la tiroxina, que se encarga de regular nuestro metabolismo.
- 29. Ayuda en la formación de los huesos, en el desarrollo de los tejidos y en la coagulación de la sangre.
- 30. Aporta un mayor equilibrio tanto mental como corporal.
- 31. Sintetiza el colesterol.
- 33. Protege las infecciones estimulando la producción de los anticuerpos.
- 34. Fomenta la generación de enzimas lo que ayuda a mejorar las funciones digestivas.
- 35. Ayuda en el funcionamiento del sistema nervioso.
- 36. Estimula la producción de estrógenos en los casos de infertilidad.
- 37. Se utiliza en tratamientos de migrañas y cefaleas.
- 38. Contribuye a cicatrizar la piel.
- 39. Refuerza el pelo y las uñas.
- 40. Actúa en los casos de rinitis y asma bronquial.
- 42. El manganeso en cantidades superiores a 5 mg/m3 es muy tóxico.
- 43. No es sirve de mucho obtener metal puro ya que las aplicaciones que tiene son escasas, y sus propiedades son inadecuadas.
- 44. Su conductividad eléctrica es un 4% de la que tiene el cobre.
- 45. El manganeso descompone el agua fría y al calentarlo arde formando tetraóxido.
- 46. Se oxida lentamente en el aire y si es pulverizado a Tº ambiente puede inflamarse.
- 47. Se disuelve en ácidos (desprendiendo hidrógeno).
- 48. Si está a Tº ambiente reacciona con los no metales de una manera lenta, pero si es a una Tº elevada, la reacción se produce más rápidamente.
- 49. Puede presentar distintos colores según el estado de oxidación en el que esté:+2 -> Rosa / +3 -> Rojo / +5 -> Azul / +6 -> Verde / +7: -> Violeta Podéis ver el manganeso en los diferentes estados de oxidación en el video que os he adjuntado en la página principal del manganeso.
- 50. OPINIÓN PERSONAL En mi opinión, este trabajo es bastante interesante ya que nos permite saber más sobre esos elementos que para nosotros eran hasta hace poco tiempo unas simples letras ordenadas en una tabla a la que llamaban “Tabla Periódica”. También nos permite participar de manera colectiva y poder realizar nuestro propio proyecto y que los demás puedan consultarla para que les sirva de ayuda. Sofía Antunes 1º Bachillerato C