PATOLOGIA ENFERMEDADES PEDIATRICAS ROBBINS
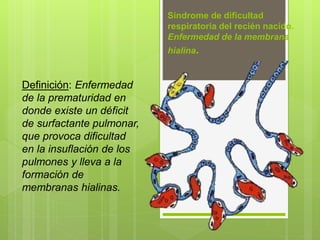
- 1. Síndrome de dificultad respiratoria del recién nacido. Enfermedad de la membrana hialina. Definición: Enfermedad de la prematuridad en donde existe un déficit de surfactante pulmonar, que provoca dificultad en la insuflación de los pulmones y lleva a la formación de membranas hialinas.
- 2. ENFERMEDADE S PEDIATRICAS Jorge Javier Galindo Cruz Gerardo Daniel Loza Magallanes Edgar Sánchez Abraham Israel García FACULTAD DE MEDICINA UADEC TORREON PATOLOGIA PATOLOGIA ROBBINS CAPITULO 7
- 4. Otras posibles influencias sobre el SDR: Cesárea Diabetes materna Embarazo gemelar
- 5. Regulación de la síntesis de surfactante HORMONAL: Las enfermedades que aumentan la liberación de Corticoides disminuyen el riesgo de desarrollar SDR. La síntesis de surfactante puede suprimirse por concentraciones sanguíneas compensadoras muy elevadas de Insulina en niños de madres diabéticas, que contrarrestan los efectos de los corticoides.
- 6. Los neumocitos tipo II se desarrollan al final del sexto mes, por lo que la producción de surfactante comienza en el tercer trimestre de la gestación.
- 7. SurfactanteFosfolípidos activos + proteínas asociadas. Dipalmitoil fosfatidil colina (lecitina). Capa de líquido + surfactante.
- 9. MorfologíaANATÓMICA • Tamaño normal • Más pesados • Menos aire • Color rojizo púrpura
- 10. HISTOLÓGICA • Aspecto sólido • Alveolos atelectásicos • Membranas hialinas eosinofílicas
- 11. Carácterísticas clínicas“Antes del surfactante exógeno ” “Después del surfactante exógeno” Prevención: • Retrasando el parto • Induciendo la madurez pulmonar fetal Las secreciones pulmonares se eliminan hacia el líquido amniótico, por lo que el análisis de los fosfolípidos del líquido amniótico supone una buena estimación de la cantidad de surfactante alveolar.
- 12. En los niños afectados es necesario el oxígeno. Sin embargo, su administración prolongada se asocia con dos complicaciones: Retinopatía de la prematuridad Pateogenia de dos fases: Hiperóxica e hipóxica Disminución en la expresión de VEFG apoptosis de células endoteliales. Restablecimiento de la concentración de VEFG neovascularización en vasos retinianos. Displasia broncopulmonar Descenso en el número de alveolos maduros. Detención del desarrollo de la septación alveolar. Aumento de TNF, e IL-8. Los niños que se recuperan de un SDR tienen mayor riesgo de desarrollar otras complicaciones como. Conducto arterioso persistente, hemorragia intraventricular y enterocolitis necrosante.
- 13. Retinoblastoma Tumor maligno más frecuente de la infancia. Incidencia disminuye con la edad Es atípico clínica y anatomopatológicamente. Generalmente congénito. Multifocal/Bilateral. Regresión espontánea. TUMORES
- 17. Células pequeñas y redondas. Núcleos grandes e hipercrómicos. Escaso citoplasma Rosetas de Flexner-Wintersteiner Puede existir Metástasis
- 18. Carácterísticas clínicas • Presentación promedio a los dos años. • Cuadro clínico -Escasa visión. -Estrabismo. -”Reflejo de ojo de gato”. -Dolor y sensibilidad ocular. • Generalmente mortales si no son tratados. • Supervivencia habitual bajo tratamiento. • Algunos desaparecen espontáneamente. • RB familiar mayor probabilidad de osteosarcomas. TUMORES
- 20. Fibrosis quística Es una enfermedad extensa de origen genético, autosómica recesiva. El daño se encuentra en el Transporte epitelial que afecta la secreción de líquidos por las glándulas exocrinas y el epitelio que recubre los tractos respiratorio, gastrointestinal y reproductor.
- 21. 1/3,200 Nacidos vivos 1 /31,000 Nacidos vivos 1/15,000 Nacidos vivos Es la enfermedad genética mortal más frecuente que afecta a la raza blanca. FIBROSIS QUÍSTICA
- 22. Las secreciones mucosas anormalmente viscosas son responsables de las dos manifestaciones clínicas más importantes: Aunque las glándulas sudoríparas son estructuralmente normales, una anomalía bioquímica característica es una concentración alta de cloruro sódico en el sudor. 1. Infecciones pulmonares recurrentes y crónicas. 2. Insuficiencia pancreática. FIBROSIS QUÍSTICA
- 23. 1. Se transmite de forma autosómica recesiva simple. 2. No afecta a los portadores heterocigotos. 3. Los afectados tienen mutaciones en ambos alelos. FIBROSIS QUÍSTICA
- 24. Existe un compendio de variaciones fenotípicas debido a: Mutaciones del gen CFTR Efectos específicos tisulares Modificadores de la enfermedad Es provocada por mutaciones en el gen CFTR que codifica el regulador transmembrana de la FQ, alterando el transporte de los iones Cloro. FIBROSIS QUÍSTICA
- 25. PATOGENIA • Ausencia total o parcial de la proteína de canal de cloro epitelial. • Codificada por el gen regulador de conductancia transmembrana de la FQ (CFTR) localizado en el cromosoma 7q31.2. • Cambios secundarios en el moco. • Membranas epiteliales relativamente impermeables a los iones Cl-. FIBROSIS QUÍSTICA
- 26. La pérdida de la función de CFTR produce la deficiencia en la reabsorción de Na y Cl y un sudor hipertónico. Las mutaciones producen una pérdida o reducción de la secreción de Cl a la luz, aumenta la absorción de Na y agua. Lo que produce una capa de líquido isotónica en los epitelios, pero de poco volumen superficial. CFTRreabsorbe ClYNa CFTRsecretaCl yabsorbeNa “El impacto de este defecto en la función de transporte es específico de tejido.” FIBROSIS QUÍSTICA
- 28. Se han identificado 800 mutaciones del gen CFTR que provocan la enfermedad. La mutación más frecuente (70% de los pacientes con FQ) produce una deleción de tres nucleótidos que codifican fenilalanina en la posición 508. (ΔF508) Se pueden clasificar según la localización de la mutación en la secuencia génica. FIBROSIS QUÍSTICA
- 29. La combinación de las mutaciones en los dos alelos influye en el fenotipo global, así como las manifestaciones específicas de cada órgano. La FQ, es un ejemplo del axioma “un gen, una enfermedad”. Sin embargo, existen modificadores genéticos que modulan la frecuencia y la gravedad de las manifestaciones. Riesgo tres veces mayor a sufrir una enfermedad pulmonar de estadio final y una menor supervivencia debida a infecciones bacterianas crónicas en el contexto de una FQ. FIBROSIS QUÍSTICA
- 30. TUMOR DE WILMS Nefroblastoma TUMORES • Tumor primario renal más frecuente. • Más casos entre los 2 y 5 años. • Conceptos de los tumores infantiles -Malformaciones congénitas asociadas - Morfología -Evolución clínica
- 31. Malformaciones congénitas asociadas Síndrome de WAGR Síndrome de Denys-Drash Síndrome de Beckwith-Wiedemann (SBW) Anomalías en el gen WT1 11p13 Gen implicado “WT2” 11p15.5 33% 90% Deleción Mutación inactivadora dominante negativa Trastorno de impronta genómica
- 33. WAGR Aniridia Anomalías genitales Retraso mental SDD Disgenesia gonadal Anomalías renales SBW Agrandamiento de órganos individuales Agrandamiento de segmentos corporales(hemihipertrofia) Agrandamiento de las células corticales suprarrenales (citomegalia adrenal) • 10 genes en un solo alelo paterno. • Silencio transcripcional homólogo parental:Metilación de la región promotora. • IGF2 es candidato por la pérdida de la impronta.
- 34. MORFOLOGÍA Masa grande Solitaria Bien delimitada Blando, homogéneo y grisáceo Hemorragia Necrosis
- 35. Histología trifásica Blastémico, estromal y epitelial
- 36. Otros elementos heterólogos raras veces. Focos de anaplasia (5%)p53 Resistencia a quimioterapia. Restos negrogénicos
- 37. TUMORES EVOLUCIÓN CLÍNICA Masa abdominal pallpable Fiebre Dolor abdominal Hematuria Obstrucción intestinal PRONÓSTICO Generalmente muy bueno Nefrectomía y quimioterapia Anaplasia (focal/difusa)
