Clase 16 ensayos clínicos
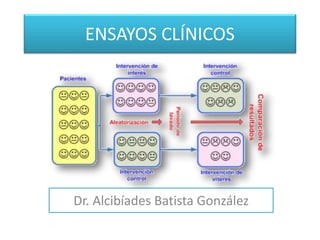
- 1. ENSAYOS CLÍNICOS Dr. Alcibíades Batista González
- 2. TEMAS A DESARROLLAR • ¿Qué es un ensayo clínico aleatorio? • ¿Cuáles son sus características? • Ventajas y desventajas de los estudios clínicos aleatorizados. • Población: – Población de referencia – Población experimental – Grupo experimental
- 3. TEMAS A DESARROLLAR • Grupo de estudio y grupo de control en los ensayos clínicos aleatorios. • ¿Por qué aleatorizar la muestra? – ¿Cómo se realiza la aleatorización? • Técnicas de ciego o enmascaramiento.
- 4. TEMAS A DESARROLLAR • Cálculo de la muestra en los ensayos clínicos aleatorios. • Poder estadístico. • Análisis de resultados. • Significancia estadística vs significancia clínica.
- 5. ¿QUÉ ES UN ENSAYO CLÍNICO ALEATORIO (ECA)? • Un ECA es un experimento prospectivo que sirve para comparar una o más intervenciones en un grupo experimental vs un grupo control. • Busca determinar la efectividad de la intervención. • Compara, por ejemplo: – Un fármaco contra placebo – Un nuevo tratamiento contra el tratamiento estándar – Una intervención Qx vs Tx médico
- 6. ¿QUÉ ES UN ENSAYO CLÍNICO ALEATORIO (ECA)? • Cualquier situación como las anteriores, en la que el experimentador escoge los grupos de tratamiento y control, a través de un sistema de aleatorización, y controla las posibles variables de confusión, puede ser considerado un ECA.
- 7. CARACTERÍSTICAS DE LOS ECA • Los ECA se definen básicamente por dos características: 1. Los investigadores tienen el control sobre el factor de estudio, es decir, deciden: Qué tratamiento Con qué pauta Durante cuanto tiempo recibirá la intervención cada uno de los grupos en estudio. 2. La asignación de los individuos se realiza en forma aleatoria.
- 8. VENTAJAS DE LOS ECA • Proporcionan un mayor control del factor de estudio. • La asignación aleatoria, o al azar, tiende a controlar los factores pronósticos que pueden influir en el resultado, incluidos aquellos que no se miden, y de este modo se aísla el efecto de la intervención. • Por ser experimentales, son los que proporcionan la mejor evidencia de una relación causa-efecto.
- 9. DESVENTAJAS DE LOS ECA • Restricciones éticas impiden muchas veces, seguir esta metodología. • Se llevan a cabo en una muestra muy seleccionada, lo que dificulta la generalización. • Las intervenciones pueden ser muy rígidas, estar muy estandarizadas – Difieren de lo que ocurre en la práctica habitual. • Abordan la relación entre una única intervención y su efecto sobre una enfermedad/condición. – Los estudios de observación analíticos pueden evaluar varios factores de riesgo.
- 10. DESVENTAJAS DE LOS ECA • Suelen tener un costo elevado, según la duración y complejidad del protocolo. • Deben tomarse en cuenta muchos factores: – Elección de la población – Asignación aleatoria – Utilidad del placebo – Técnicas de enmascaramiento – Seguimiento de los participantes – Aspectos éticos
- 11. Población Criterio de selección Población Experimental Participantes Grupo de estudio: Intervención A No participantes Grupo control: Intervención B/Placebo Consentimiento Aleatorización Pérdidas Pérdidas No cumplidores No cumplidores Reacciones adversas Reacciones adversas Comparación Respuestas Respuestas Resultados Análisis e interpretación Conclusiones Modificado de: Nativí N, José N. (Editor) (2000). Introducción a la investigación científica. 1ª Edición. Panamá. Editora Sibauste.
- 12. POBLACIÓN… ENSAYOS CLÍNICOS ALEATORIOS
- 13. POBLACIÓN DE REFERENCIA • Es aquella población hipotética que comprende tanto los grupos presentes, como los grupos pasados y futuros, a los cuales se proyecta inferir las conclusiones del estudio o a los cuales se espera que las conclusiones puedan ser aplicables. • La población de referencia podría ser: – Toda la humanidad – La población de una región o de un país – La totalidad o parte de la población general del área dónde se realiza el estudio
- 14. Estudio de Fase III Rota 023 18 Sitios en 12 Países República Dominicana 4056 (6.4%) México 13245 (20.9%) Venezuela 4250 (6.7%) Brazil 3218 (5.1%) Total: 63,225 59,308 (93.8%) Honduras 4195 (6.6%) Nicaragua 4057 (6.4%) Panamá 4061 (6.4%) Chile 3458 (5.5%) Argentina 4671 (7.4%) Colombia 3910 (6.2%) Perú 12044 (19.0%) Finlandia 2060 (3.3%) Ref: Vesikari T et al ESPID 2005, Abstract 31 10 Auditorias = 0 hallazgos críticos
- 15. POBLACIÓN EXPERIMENTAL • Es aquella en la que se ejecuta el estudio o en la cual se hace la evaluación. • Generalmente es una fracción o parte real de la población de referencia. • La población experimental debe: – Ser suficientemente grande – Estar muy bien definida – Ser representativa de la población de referencia
- 16. GRUPO EXPERIMENTAL • De la población experimental se toma un grupo de personas que: – Llenen todos los requisitos para participar en la investigación – Consientan participar en el ECA • Una vez definido el grupo experimental, se subdividirá en dos grupos, mediante un proceso al azar: – Grupo de control – Grupo de estudio
- 17. GRUPO DE ESTUDIO Y GRUPO CONTROL… ENSAYOS CLÍNICOS ALEATORIOS
- 18. GRUPO DE ESTUDIO Y GRUPO CONTROL • El grupo de estudio y el grupo control o testigo se forman a partir del grupo experimental. • Es esencial que el grupo control sea lo más similar al grupo de estudio. – Esto asegura que las diferencias en los resultados se puedan atribuir al tratamiento o fármaco en estudio, y no a las diferencias en las características de los dos grupos.
- 19. GRUPO DE ESTUDIO Y GRUPO CONTROL • Grupo de estudio: – Es el grupo de participantes que recibirá la droga o se someterá al tratamiento que se está estudiando. • Grupo control o testigo: – Es el grupo de participantes que recibe el placebo o el tratamiento estándar, dependiendo del caso.
- 20. FORMACIÓN DE LOS GRUPOS • El grupo de pacientes designados como grupo experimental debe cumplir con ciertos criterios estipulados por el investigador. – Criterios de inclusión – Criterios de exclusión • Debe buscarse la máxima similitud entre los participantes. • Los criterios deben estipularse antes de crear el grupo de control y el de estudio.
- 21. FORMACIÓN DE LOS GRUPOS • En cuanto a la asignación a los grupos de control o de estudio, debe considerarse y establecerse cuando se va a dar la entrada al experimento: – Entrada común para todos los individuos que van a participar – Entrada individual, a lo largo del tiempo, a medida que se presentan los individuos seleccionados – Entrada en forma sucesiva por subgrupos.
- 22. ¿POR QUÉ ALEATORIZAR? • El principio básico de todo ensayo clínico, y de todas las investigaciones científicas, es reducir al mínimo los sesgos de selección e información. – Cuando no se sabe qué variable afecta o pudiese afectar los resultados de un experimento, la mejor manera de reducir sesgos de selección, es asignar a los individuos a los grupos de control y estudio, mediante un proceso de aleatorización. – La meta es asegurar una distribución igual de las variables entre los grupos de individuos a estudiar.
- 23. ¿POR QUÉ ALEATORIZAR? • Cuando se trabaja y se sabe con certeza que alguna de las variables involucradas, que no es la que se está estudiando, afecta el resultado, se puede entonces: – Agrupar o estratificar la muestra inicialmente, para luego proceder a aleatorizar. • Dos ejemplos muy comunes de variables que hacen necesaria una estratificación son la edad y el sexo de los individuos participantes en el ensayo.
- 24. PROCEDIMIENTO DE ALEATORIZACIÓN • La asignación al azar significa que todos y cada uno de los participantes tienen igual probabilidad de pertenecer a cualquiera de los grupos. • Se utilizan: – Tablas de números aleatorios – Software especializado, etc.
- 25. TÉCNICAS DE CIEGO O ENMASCARAMIENTO • Es otra forma de reducir los segos en ensayos clínicos. • Se pueden utilizar los métodos: – Ciego simple – Doble ciego – Triple ciego • Reducen los sesgos de información que pueden ser producidos por la observación. – Se busca que la percepción subjetiva del investigador y/o participantes, no influya en la interpretación de los resultados.
- 26. TÉCNICAS DE CIEGO O ENMASCARAMIENTO • Simple ciego o simple anonimato: – En este método los individuos participantes desconocen si forman parte del grupo de estudio o de control. • Doble ciego o doble anonimato: – Es el método en el que ni los investigadores ni los individuos, saben quién pertenece al grupo de estudio o de control. • Triple ciego o triple anonimato: – Tiene las características consignadas en el doble ciego; pero, además el estadístico que va a analizar los datos, desconoce también la asignación.
- 27. TÉCNICAS DE CIEGO O ENMASCARAMIENTO • Al final del ensayo, cuando se van a comparar los resultados (o después de comparados en el triple ciego), se descubren los dos grupos para ver cual era el grupo de estudio y cual el grupo control, y quiénes pertenecía a cada grupo. • En muchos ensayos, se realizan evaluaciones y auditorías en el transcurso del experimento. – Detectar violaciones al protocolo no reportadas – Alteración de datos o resultados – Necesidad de romper el ciego y detener el estudio
- 28. En 1994, se aplicó la prueba o método de Kaplan-Meier a los resultados acumulados del ensayo. Se estimó que la proporción de transmisión de VIH-1 para niños que recibieron placebo era del 22.6% comparado con el 7,6% de los que recibieron AZT (una reducción del 66% del riesgo de transmisión). El estudio se detuvo, pues no era ético continuarlo. Se recomendó iniciar la administración de AZT a toda embarazada infectada con VIH, a partir de la semana 14 de gestación.
- 29. TAMAÑO DE LA MUESTRA • Para el cálculo del tamaño de la muestra, en los ensayos clínicos aleatorios, es necesario conocer ciertas definiciones: 1. Magnitud del efecto o “effect size” 2. Poder estadístico a. Nivel de significancia b. Probabilidad de error tipo II c. Poder
- 30. 1. MAGNITUD DEL EFECTO • ¿Cuándo una diferencia en el efecto es pequeña? ¿Cuándo es adecuada? • El tamaño de la diferencia que queremos (o esperamos) detectar es llamado magnitud del efecto (“effect size”). • Para calcular el tamaño de la muestra, necesitamos saber la mínima diferencia que esperamos encontrar entre los dos grupos. • ¿Qué tan seguro quiere estar de poder encontrar la diferencia, si existe? – Eso dependerá del poder estadístico que utilice para su estudio.
- 31. 2. PODER ESTADÍSTICO • El poder estadístico representa la probabilidad de encontrar la magnitud del efecto real. • Está relacionado con el nivel de significancia, con el error tipo I y el error tipo II. a. Nivel de significancia: es la probabilidad de un error tipo I o error α. b. Probabilidad de error tipo II o β. c. Poder = 1-β Es la probabilidad de encontrar la magnitud del efecto cuando realmente lo hay.
- 32. TAMAÑO DE LA MUESTRA • Para calcular el tamaño de la muestra se debe especificar: – Magnitud del efecto esperado – El nivel de significancia – El poder estadístico deseado • Mientras más bajo mantengamos el nivel de los errores tipos I y II: – El tamaño de la muestra será más grande – El poder estadístico será mayor
- 33. TAMAÑO DE LA MUESTRA • Para calcular el tamaño de la muestra se usa la siguiente fórmula: 푛 = 푝1푞1 + 푝2푞2 푝2 − 푝1 2 ∗ ∫ 훼, 푝표푑푒푟 Donde: n = # de pacientes por grupo p1 = porcentaje esperado en grupo 1 (control) p2 = porcentaje esperado en grupo 2 (estudio) q1 = 1 – p1 q2 = 1 – p2 α = nivel de significancia ƒ(α, poder) = valor se obtiene de una tabla
- 34. TABLA DE VALORES DE ƒ(α, poder) PODER (1 – β) 0.95 .90 .80 NIVEL DE SIGNIFICANCIA O ALPHA (α) 0.10 10.8 8.6 6.2 0.05 13.0 10.5 7.9 0.01 17.8 14.9 11.7
- 35. Estudio de Fase III Rota 023 18 Sitios en 12 Países República Dominicana 4056 (6.4%) México 13245 (20.9%) Venezuela 4250 (6.7%) Brazil 3218 (5.1%) Total: 63,225 59,308 (93.8%) Honduras 4195 (6.6%) Nicaragua 4057 (6.4%) Panamá 4061 (6.4%) Chile 3458 (5.5%) Argentina 4671 (7.4%) Colombia 3910 (6.2%) Perú 12044 (19.0%) Finlandia 2060 (3.3%) Ref: Vesikari T et al ESPID 2005, Abstract 31 10 Auditorias = 0 hallazgos críticos
- 36. ENSAYO CLÍNICO CRUZADO • Hasta ahora, hemos descrito estudios en paralelo. – Cada paciente recibe solamente una intervención, dependiendo del grupo al que pertenezca. – Los resultados obtenidos en cada uno de los grupos, se comparan entre sí. – El análisis se basa en las diferencias en los resultados obtenidos en cada grupo.
- 37. ENSAYO CLÍNICO CRUZADO • El diseño cruzado (“cross-over”) es una forma especial de ECA menos utilizada. • En estos ECA, cada sujeto actúa como su propio control. • Un diseño sencillo sería que cada individuo del grupo experimental recibe al azar una de las dos intervenciones y, en un segundo período, recibe la otra. – Ambos periodos están separados por una fase de blanqueo para permitir que el paciente vuelva a su estado inicial, desapareciendo el efecto del Tx administrado en el primer periodo.
- 38. Población experimental Consentimiento Participantes Modificado de: Nativí N, José N. (Editor) (2000). Introducción a la investigación científica. 1ª Edición. Panamá. Editora Sibauste. Grupo 1 (A) Grupo 2 (B) Respuesta A1 Respuesta B1 Periodo de blanqueo Grupo 2 (A) Grupo 1 (B) Respuesta A2 Respuesta B2 Comparación de resultados (A1+A2) (B1+B2)
- 39. ENSAYO CLÍNICO CRUZADO • Además del efecto propio de la intervención en estudio, dentro del diseño cruzado, se pueden dar dos tipos más de efectos, que dificultan enormemente la interpretación de los resultados del ensayo: 1. Efecto de periodo 2. Efecto de secuencia
- 40. ENSAYO CLÍNICO CRUZADO Grupo 1 Secuencia 1 Grupo 2 Secuencia 2 Total Período 1 A1 B1 A1 + B1 Período 2 B2 A2 A2 + B2 Total A1 + B2 B1 + A2 • Efecto de intervención: comparación de los resultados obtenidos por el fármaco A, con los obtenidos por el fármaco B. (A1+A2) frente a (B1+B2). • Efecto período: comparación de los resultados obtenidos por ambos fármacos en el período 1, con los obtenidos en el período 2. (A1+B1) frente a (A2+B2) • Efecto secuencia: comparación de los resultados obtenidos al administrar los fármacos según la secuencia 1 con los obtenidos al administrarlos en la secuencia inversa (A1 + B2) frente a (B1 + A2).
- 41. ENSAYO CLÍNICO CRUZADO 1. Efecto período: Dado que cada paciente se observa en dos períodos distintos, es importante determinar si ha existido algún cambio entre el primero y el segundo. La enfermedad o síntoma progresa, regresa, fluctúa en su gravedad Una manera de minimizar este efecto es que cada paciente cambie de tratamiento varias veces. Ello dificulta la ejecución y aceptación.
- 42. ENSAYO CLÍNICO CRUZADO 2. Efecto secuencia: los pacientes reciben una secuencia de tratamientos, dependiendo del grupo en el que estén. El efecto residual del tratamiento recibido en el primer período, puede afectar la respuesta. El efecto residual puede estar presente aunque el período de blanqueo sea lo suficientemente largo. El efecto residual puede incluir efectos psicológicos.
- 43. ENSAYO CLÍNICO CRUZADO • Ventajas: – Es más eficiente que un estudio en paralelo, ya que se requiere un número menor de participantes. – Cada participante es su propio control, por lo que se pueden utilizar técnica estadísticas para datos apareados que son más potentes.
- 44. ENSAYO CLÍNICO CRUZADO • Limitaciones: – Mayor duración que los estudios en paralelo. – No puede utilizarse en enfermedades agudas o cuya evolución cursa a brotes. – No se puede aplicar cuando no es posible asegurar la desaparición del efecto de la primera intervención en todos los participantes.
- 45. ANÁLISIS DE LOS RESULTADOS • En los ECA se trata de encontrar si la diferencia entre la frecuencia del efecto (la enfermedad), en el grupo de estudio y de control, es significativa. • Se quiere sustentar que, en un grupo de estudio, comparado con el grupo control: – La medida preventiva en estudio es efectiva o no – La droga es o no eficaz – El factor de riesgo manipulado aumenta o no la frecuencia del efecto
- 46. ANÁLISIS DE LOS RESULTADOS • Siempre es probable que, en los ECA, se produzca la pérdida de algunos pacientes en el seguimiento. • Mientras más pacientes se pierdan y menos se sepa acerca de ellos, menos confianza podrá tenerse en los resultados del estudio. – Intención a tratar – Análisis por protocolo
- 47. ANÁLISIS DE LOS RESULTADOS • Análisis por “intención a tratar”: en el análisis de los resultados, los pacientes deberán permanecer en el grupo de tratamiento (estudio o control) originalmente asignado para el ensayo, inclusive en el caso de que reciban otro tratamiento, si el régimen original falla. • Si removemos a los “no cumplidores del protocolo” del análisis, esto puede limitar la capacidad del ensayo para generar los hallazgos que se desea encontrar y generalizarlos a la práctica clínica. • La cuestión esencial es tener la información sobre el resultado entre todos los pacientes que recibieron el Tx y no solo entre aquellos que lo completaron.
- 48. ANÁLISIS DE LOS RESULTADOS • Para presentar el informe de un ECA, debe asegurarse de incluir los datos primarios suficientes que permitan al lector: – Comparar las características de los grupos – Efectuar pruebas estadísticas básicas para determinar si el azar puede excluirse de modo razonable, como causa de las diferencias entre los grupos que se están comparando.
- 49. ANÁLISIS DE LOS RESULTADOS • En muchos ECA, los resultados tiene respuesta de sí/no: – Se curó/no se curó – Descendió un marcador/no descendió – Hubo recurrencia/no hubo recurrencia • Cuando este es el caso, los resultados pueden desplegarse en un formato de tabla, bastante sencillo, para su análisis.
- 50. ANÁLISIS DE LOS RESULTADOS RETINOPATÍA TRATAMIENTO ESTÁNDAR TRATAMIENTO INTENSIVO TOTAL Sí 91 23 114 No 287 325 612 Total 378 348 726 Modificado de: Nativí N, José N. (Editor) (2000). Introducción a la investigación científica. 1ª Edición. Panamá. Editora Sibauste. 1. Tasa de incidencia: la tasa de incidencia de retinopatía para c/grupo de tratamiento, se determina dividiendo el número de sujetos que desarrollaron retinopatía, entre el número de pacientes-años del seguimiento. El factor pacientes-años de calculó sumando los años que cada sujeto tenía en el estudio, previo al desarrollo de retinopatía. Esto permite incluir a todos los sujetos en los resultados de un estudio, sin importar cuanto tiempo tenía enrolado cada paciente (el reclutamiento de sujetos sucedes a menudo en varios años).
- 51. ANÁLISIS DE LOS RESULTADOS 2. Porcentaje de incidencia / Porcentaje de reducción de tasa: una manera de comparar las tasas de incidencia en cada grupo, es calcular el porcentaje de incidencia que lograríamos evitar con la intervención. Ese porcentaje se conoce como “reducción de tasa” y se calcula: Reducción de tasa = (Ti estándar – Ti experimental )/ Ti estándar x 100 Si el porcentaje de reducción de tasa es igual a cero, no hay reducción en la tasa de incidencia atribuible al nuevo Tx, ambas intervenciones son equivalentes. Mientras más alejado del cero se encuentre el porcentaje de reducción de tasa, mayor es la diferencia entre los dos grupos
- 52. ANÁLISIS DE LOS RESULTADOS 3. Proporción de tasas: otro método de comparar 2 tasas es formando una proporción de tasas. Es útil para situaciones donde se estiman los riesgos, más que las tasas de los eventos. También puede estimarse como riesgo relativo riesgo en el grupo experimental entre riesgo en el grupo control. Se le puede llamar proporción de riesgo o riesgo relativo. Reducción de tasa = Ti experimental / Ti estándar Sí la proporción de riesgo es igual a 1.0, no hay diferencia entre los grupos. Mientras más lejos esté de 1, mayor la diferencia. Se pueden calcular los límites de confianza al 95%
- 53. ANÁLISIS DE LOS RESULTADOS 4. Comparación de medias: cuando los valores no son dicotómicos, entonces recurrimos a la media aritmética (promedios). Aquí el objetivo es rechazar la Ho, para aceptar la Ha. La Ho sería que las medias en ambos grupos son iguales. Al negar la Ho, se acepta la Ha: las medias no son iguales. Para probar la igualdad de las medias, se efectúa la prueba de t para medias ponderadas. Una vez obtenido el valor de t, se busca el valor de p correspondiente. Un valor de p < 0.05 nos indica que la diferencia entre las medias es poco probable que se deba al azar o a la variabilidad del muestreo (se rechaza la hipótesis nula).
- 54. SIGNIFICANCIA ESTADÍSTICA / SIGNIFICANCIA CLÍNICA • Una vez que encontremos o no una diferencia estadísticamente significativa entre un tratamiento estándar y un tratamiento experimental, debemos decidir si este hallazgo es clínicamente significativo. • ¿Existe diferencia entre significancia clínica y significancia estadística?
- 55. Para ver el video proyectado en clase, vaya a la dirección: http://youtu.be/PrQDYNk4C U0
- 56. BIBLIOGRAFÍA • Fathalla, Mahmoud F.; Fathalla, Mohamed M.F. (2004). Guía práctica de investigación en salud. Washington, D.C. Organización Panamericana de la Salud. Publicación científica y técnica No. 620. • Hernández Sampieri, Roberto; Fernández C., Carlos; Baptista L., Pilar (2003). Metodología de la investigación. 3ª Edición. México. McGraw- Hill/Interamericana Editores, S.A. de C.V. • Nativí N, José N. (Editor) (2000). Introducción a la investigación científica. 1ª Edición. Panamá. Editora Sibauste. • Pineda, Elia B.; de Alvarado, Eva L.; de Canales, Francisca H. (1994). Metodología de la investigación. Manual para el desarrollo de personal de salud. 2ª Edición. Washington, D.C. Organización Panamericana de la Salud. Serie PALTEX para ejecutores de programas de salud No. 35.
