Segunda energía ionización átomos
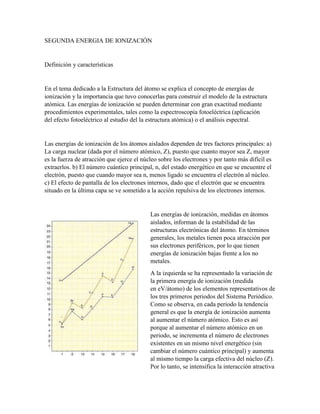
- 1. SEGUNDA ENERGIA DE IONIZACIÓN Definición y características En el tema dedicado a la Estructura del átomo se explica el concepto de energías de ionización y la importancia que tuvo conocerlas para construir el modelo de la estructura atómica. Las energías de ionización se pueden determinar con gran exactitud mediante procedimientos experimentales, tales como la espectroscopia fotoeléctrica (aplicación del efecto fotoeléctrico al estudio del la estructura atómica) o el análisis espectral. Las energías de ionización de los átomos aislados dependen de tres factores principales: a) La carga nuclear (dada por el número atómico, Z), puesto que cuanto mayor sea Z, mayor es la fuerza de atracción que ejerce el núcleo sobre los electrones y por tanto más difícil es extraerlos. b) El número cuántico principal, n, del estado energético en que se encuentre el electrón, puesto que cuando mayor sea n, menos ligado se encuentra el electrón al núcleo. c) El efecto de pantalla de los electrones internos, dado que el electrón que se encuentra situado en la última capa se ve sometido a la acción repulsiva de los electrones internos. Las energías de ionización, medidas en átomos aislados, informan de la estabilidad de las estructuras electrónicas del átomo. En términos generales, los metales tienen poca atracción por sus electrones periféricos, por lo que tienen energías de ionización bajas frente a los no metales. A la izquierda se ha representado la variación de la primera energía de ionización (medida en eV/átomo) de los elementos representativos de los tres primeros periodos del Sistema Periódico. Como se observa, en cada periodo la tendencia general es que la energía de ionización aumenta al aumentar el número atómico. Esto es así porque al aumentar el número atómico en un periodo, se incrementa el número de electrones existentes en un mismo nivel energético (sin cambiar el número cuántico principal) y aumenta al mismo tiempo la carga efectiva del núcleo (Z). Por lo tanto, se intensifica la interacción atractiva
- 2. entre el electrón menos ligado y el núcleo. Por estas razones, los metales alcalinos (grupo I) son los elementos con menor energía de ionización. En el extremo opuesto, los gases nobles son, con mucho, los elementos con mayor energía de ionización, al tener las estructuras electrónicas más estables. Respecto a la variación de la primera energía de ionización dentro de cada familia, la tendencia general es que dicha energía disminuye al aumentar el número atómico. Al aumentar el número atómico dentro de una familia, aumenta el número de niveles y cambia el número cuántico principal. El último electrón está a una distancia mayor del núcleo y el resto de electrones (más internos) ejercen sobre él un gran poder de apantallamiento. Aunque también aumenta la carga nuclear, la intensidad de la interacción núcleo-electrón se resiente. El gráfico de la izquierda muestra la variación de la energía de ionización en los elementos alcalinos. En las otras familias, la tendencia es análoga. Nos referimos ahora a las energías de ionización posteriores a la primera (recuérdese que la primera energía de ionización es la mínima energía que hay que suministrar a un átomo neutro, en su estado fundamental, para arrancarle el primer electrón; la segunda energía de ionización es la energía precisa para sustraer el segundo electrón y así sucesivamente). Lógicamente, la primera energía de ionización, que corresponde a la extracción del electrón más alejado del núcleo, es la menor; la segunda es mayor que la primera; la tercera mayor que la segunda; y así sucesivamente. A medida que se extraen electrones, los que quedan son más atraídos por el núcleo (que no cambia), puesto que se encuentran más próximos a él, y sufren menos repulsión por el apantallamiento de los electrones restantes, colocados por debajo de ellos.
- 3. La segunda energía de ionización ( , que supone la extracción del segundo electrón, es superior a la primera porque el átomo se ha convertido previamente en un catión (con carga positiva) y su atracción por el electrón será mayor oponiendo mayor resistencia a su extracción. Esto es, es más difícil extraer un electrón de un ión cargado positivamente (e.g. que de un átomo neutro ( ). El valor de la energía de ionización está fuertemente condicionado por el tipo de configuración electrónica que se destruye al arrancar el electrón. Por ejemplo la segunda energía de ionización de los metales alcalinos es relativamente mayor que la de otros elementos porque supone la destrucción del octeto de la penúltima capa, el cual es especialmente estable. Por ello las diferencias de energía de ionización para sucesivas etapas de extracción electrónica varia enormemente de un elemento a otro. Por ejemplo la extracción del segundo electrón del ión sodio ( ) requiere diez veces más de energía que para remover el primero del átomo neutro de sodio ( ) (4562 versus 496 kJ/mol), pero la extracción del segundo electrón del magnesio requiere solo dos veces más de energía que el primero (1451 versus 738 kJ/mol). La segunda energía de ionización representa la energía necesaria para arrancar un segundo electrón y su valor es siempre mayor que la primera, ya que el volumen de un ión positivo es menor que el del átomo neutro y la fuerza electrostática es mayor en el ión positivo que en el átomo, ya que se conserva la misma carga nuclear: X+ + 2ªE.I. X2+ + e- Puedes deducir tú mismo el significado de la tercera energía de ionización y de las posteriores. La energía de ionización se expresa en electrón-voltio, julios o en Kilojulios por mol (kJ/mol).
- 4. 1 eV = 1,6.10-19 culombios . 1 voltio = 1,6.10-19 julios En los elementos de una misma familia o grupo la energía de ionización disminuye a medida que aumenta el número atómico, es decir, de arriba abajo. En los alcalinos, por ejemplo, el elemento de mayor potencial de ionización es el litio y el de menor el francio. Esto es fácil de explicar, ya que al descender en el grupo el último electrón se sitúa en orbitales cada vez más alejados del núcleo y, además, los electrones de las capas interiores ejercen un efecto de apantallamiento frente a la atracción nuclear sobre los electrones periféricos por lo que resulta más fácil extraerlos. En los elementos de un mismo periodo, la energía de ionización crece a medida que aumenta el número atómico, es decir, de izquierda a derecha. Esto se debe a que el electrón diferenciador está situado en el mismo nivel energético, mientras que la carga del núcleo aumenta, por lo que será mayor la fuerza de atracción y, por otro lado, el número de capas interiores no varía y el efecto de apantallamiento no aumenta. Sin embargo, el aumento no es continuo, pues en el caso del berilio y el nitrógeno se obtienen valores más altos que lo que podía esperarse por comparación con los otros elementos del mismo periodo. Este aumento se debe a la estabilidad que presentan las configuraciones s2 y s2p3, respectivamente. La energía de ionización más elevada corresponde a los gases nobles, ya que su configuración electrónica es la más estable, y por tanto habrá que proporcionar más energía para arrancar un electrón. Puedes deducir y razonar cuáles son los elementos que presentan los valores más elevados para lasegunda y tercera energías de ionización.