Tabla periodica xp
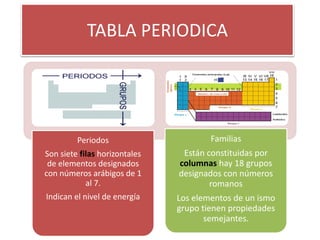
- 1. TABLA PERIODICA Periodos Son siete filas horizontales de elementos designados con números arábigos de 1 al 7. Indican el nivel de energía Familias Están constituidas por columnas hay 18 grupos designados con números romanos Los elementos de un ismo grupo tienen propiedades semejantes.
- 2. Elementos que pertenecen al mismo grupo tiene la misma configuración electrónica en su ultimo nivel Cabe destacar que existe una fuerte relación entre la configuración electrónica de los elementos y su ubicación en la tabla periódica
- 3. Primer periodo: Comprende solo dos elementos H y He elementos gaseosos mas ligeros en la naturaleza Segundo periodo: Consta e ocho elementos comienza en el litio y termina en el neón. En este periodo se ubica El O, C y N PERIODOS
- 4. Tercer Periodo: Comprende solo 8 elementos se inicia en el Na y termina en el Ar en este grupo aparece el Fosforo(P), y Azufre(S) elemento importantes en la síntesis de ácidos nucleicos y proteínas Cuarto Periodo: Comprende 18 elementos Comienza en Potasio (K) hasta el Kriptón (Kr), se encuentran metales , litio (Li),cobre (Cu), cobalto (Co), hierro (Fe), importantes en la industria PERIODOS
- 5. Quinto periodo: Tambien con 18 elementos comienza Rubidio (Rb) y termina en el Xenón (Xe), en esta serie se destaca el Yodo (Y) por su valor biológico. Sexto periodo: Tiene 32 elementos se inicia en el Cesio (Cs), y termina en el Radón (Rn) se destaca el Oro (Au) y el Platino (Pt) y el mercurio el único metal liquido que existe en la naturaleza PERIODOS
- 6. En este periodo hay un conjunto en perticular de 14 elementos llamados serie de los lantanidos (propiedades semejantes a las del lantano.) Séptimo periodo: se extiende desde el Francio(Fr), hasta el elemento ununoctio 118.En esta serie incluye 14 elementos denominados actínidos por sus propiedades semejantes al lactinio. PERIODOS
- 7. Resolución de Problemas 1, Responde: ¿ En que se diferencian la tabla periódica de Mendeleiev y tabla periódica actual? 2, Elabora una lista con los elementos que conozca y relaciónalas con productos que utilices en la vida diaria
- 9. REGIONES DE LA TABLA PERIODICA
- 10. La tabla periódica esta constituida por 4 regiones que son:
- 13. Realizar actividad de la pág. 51 del libro
- 14. CARACTERISTICAS GENERALES DE LOS GRUPOS Permite separar metales y no metales por medio de una línea escalonada los elementos a la izquierda y centro son metales mientras que los de la derecha son no metales los elementos adyacentes son metales a excepción del aluminio
- 15. El numero de electrón de valencia en los elementos representativos, el numero romano del grupo o el ultimo digito del mismo representan la cantidad de electrones de valencia de los elementos que pertenecen a dicho grupo. Ejemplo: el Azufre que tiene 6 electrones de valencia Existe manera grafica de representar a los electrones (Lewis) con puntos o líneas los cuales son ubicados alrededor del elemento corresponde al electrón de valencia.
- 16. Permite identificar el carácter metálico de los elementos representativos el mismo aumenta de arriba abajo dentro de cada grupo. Ejemplo: En el grupo 15 el (N) y el fosforo (P) son no metales mientras que el arsénico (As) y el antimonio (Sb) son semimetales para terminar con el bismuto (BI) como metal. Los elementos pertenecientes al mismo grupo tiene configuraciones electrónicas y propiedades similares.
- 17. Grupo IA Metales Alcalinos Hidrogeno no es metal Al ser el elemento mas pequeño debe de encabezar la tabla. Tiene su electrón en el ultimo nivel de energía Son metales, livianos Tiene facilidad para oxidarse y reaccionar violentamente con el H2O para formar bases y con los halógenos para formar sales
- 18. Grupo IIA Metales Alcalinotérreos Poseen en su ultimo nivel dos electrones Son metales duros y plateados reaccionar con el H2O para formar bases pero no tan fuerte como los alcalinos y con los halógenos para formar sales Punto de fusión y ebullición mayor al de los alcalinos Magnesio: piezas para carros Calcio: fabricación de yeso Bario: radiografías Radio. radioterapia
- 19. Grupo VIIA: Halógenos Tiene la capacidad de formar sales. A temperatura ambiente los dos primeros son gases El tercero es un no metal liquido Y los dos últimos son solidos Cl, F, Y son importantes para el funcionamiento del organismo. Cl (acido Gástrico) F (esmalte dental) Y (funcionamiento de las tiroides) Br (películas fotográficas) As (radiactivo)
- 20. Grupo VIII A: Gases Nobles Se caracteriza por su inactividad química debido a su gran estabilidad. El xenón y radón estos gases fueron los últimos en descubrirse formando parte de la atmosfera en pequeñas cantidades. Neón: en anuncio de luces brillantes. Helio: refrigerante Radón: cáncer Xenón: bombillas y lámparas.
- 22. Propiedades periódicas de los Elementos La tabla periódica Incremento de su numero atómico Caracterís ticas físicas y químicas Las propiedades que se repite de forma secuencial Periodicida d
- 23. RADIO ATOMICO Se define como la mitad de la distancia entre dos núcleos de un mismo elemento unidos entre si. Estas distancia se calculan mediante técnicas de refracción de rayos x, neutrones o electrones Aumenta en los grupos de arriba hacia abajo Aumenta en los periodos de izquierda a derecha Esto se debe a que los elementos que presentan mayor carga nuclear atrae a los electrones disminuyendo su radio.
- 24. Disminución del radio atómico Aumento del radio atómico TENDENCIA DEL RADIO ATOMICO EN LOS GRUPOS Y PERIODOS
- 25. RADIO IONICO Cuando el átomo de un elemento pierde un electrón se convierte en ion positivo (catión) El tamaño del ion es menor al átomo neutro. Cuando el átomo de un elemento gana un electrón se convierte en ion negativo (anión ) El tamaño del ion es mayor al átomo neutro. Átomo Na 1,86 Catión Na 0,95 Átomo F 0,64 Anión F 1,36 El tamaño que tiene un elemento luego de haber ganado o perdido un electrón con el fin de adquirir la configuración electrónica del gas noble mas cercano.
- 26. Electronegatividad Es la capacidad relativa de un átomo de ese elemento para atraer electrones hacia sí, cuando forma parte de un enlace químico. El valor esta dado por la escala Pauling F= 4 (mas alto) Fr= 0,7(mas bajo) La electronegatividad disminuye de arriba hacia abajo en los grupos y aumenta de izquierda a derecha en os periodos
- 27. Energía de ionización: Es la suficiente energía que hay que suministrar a un átomo neutro en estado gaseoso para arrancarle el electrón mas externo Aumenta de abajo hacia arriba en los grupos y de izquierda a derecha en los periodos
- 28. Predicciones de Formulas mediante el uso de tabla periódica Para predecir la formula del cloruro de sodio Na = 1 e su ultimo nivel Cl= 7 e en su ultimo nivel Para cumplir con la ley del octeto pues la formula se escribe así pues lo elementos mas electropositivos se escriben primero.