O2
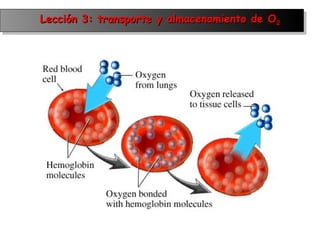
- 1. Lección 3: transporte y almacenamiento de O 2
- 2. Origen y evolución de la vida eones (miles de millones de años) tierra vida atmósfera O 2 organismos plucicelulares 4.5 3.5 2.5 0.5 CH 4 , NH 3 , Fe 2+ , S = CH 4 , NH 3 , Fe 2+ , S = +O 2 O 2 , N 2 , Fe 3+ , CO 2 depósitos de Fe 2 O 3 0 O 2 cte
- 3. O 2 : enlace y reactividad química 2s 2s 2p 2p 2s 2s * 2p 2p * 2p 2p * d O-O 1.2 Å (OE=2) tendencia a reducirse O 2 = O 2 oxidante fuerte cinéticas lentas O 2 se enlaza de forma no lineal 2p * HOMO 2p * HOMO X O 2 singlete más oxidante que el fundamental 2p * HOMO M n+ ,R· R
- 5. Transporte y almacenamiento de O 2
- 6. Transporte y almacenamiento de O 2 Protoporfirina IX Hemoglobina y Mioglobina en la mayoría de los organismos
- 7. Hemeritrina Hemocianina Artrópodos y moluscos algunos invertebrados marinos
- 8. Mioglobina Mb Mb= globina + propoforfirina IX Sólo 6% Fe es Mb 1Mb:1O 2 Difusión final similar al O 2 libre No muy eficaz?
- 9. Estructura de la Mioglobina globina Protoporfirina IX Mr 18KDa
- 10. O 2 O 2 Estado de oxidación del Fe? Esfera de coordinación? Configuración de espín del Fe? Histidina próxima Fe(II) C 4v HS 2 Å 0.4 Å N N N N N O O Fe-O-O 115º O 2 desoxi Mb oxi Mb N N N N N
- 11. Mecanismo fijación O 2 N N N N N desoxi Mb O 2 N N N N N oxi Mb O O Fe-O-O 115º Fe(II) LS - 1 O 2 Fe(III) LS - 2 O 2 ·- Weiss Pauling & Coryell
- 12. Fe(II) LS - 1 O 2 Fe(III) LS - 2 O 2 ·- Weiss Pauling & Coryell experimental 1100cm -1 típica de O 2 ·- Mossbauer más típico de Fe(III) [Co(Hb)] EPR S=1/2 de O 2 ·- Diamagnético S=0 interacción antiferromagnética Diamagnético S=0 No e - desapareados Hb-O 2 + CO Hb-CO Reacciones de Fe(II) y no Fe(III)
- 13. Histidina próxima H Histidina distal Val Phe O O
- 14. El papel no inocente de la globina His próxima H His distall Val Phe H 2 O, OH - X O O Afinidad de CO-heme es 2500 afinidad O 2 -heme En Mb sólo 250 En Mb-CO Fe-C-O no es lineal - O(O 2 ) > - O(CO) Evitar oxidación irreversible a meta-Mb: embudo hidrofóbico. O O O C
- 15. Hemoglobina Hb 4 x Mb PM=64.5 KDa Puentes salinos entre Subunidades
- 16. Mb versus Hb Hb 1 + 2 + 1 + 2 Efecto cooperativo Alosterismo: influencia pH, CO 2 , Cl - Alosterismo homotrópico (O 2 ) Alosterismo heterotrópico (CO 2 ) pH pO 2 6 Hb Mb
- 17. “Trasvase” de O 2 desde Hb a Mb
- 18. “Trasvase” de O 2 desde Hb a Mb pO 2 lungs > T-state O 2 affinity T-state R-state + H + CO 2 (músculo) H 2 CO 3 glucosa(músculo) ácido láctico pH O 2 -Hb O 2 -Mb Efecto Bohr
- 20. Hemeritrina deoxyHr: 2 HS Fe(II) oxyHr: redox reaction O 2 = (HO 2 - ) HS Fe(III) dFe-Ooxo 1.78Å dFe-O 2-2.20Å antiferromagnetic coupling (J=-77cm -1 ) Compuestos modelos Otros sitios Fe 2 : MMO. O 2 glu asp his his his his his
- 21. Modelos del sitio activo de hemeritrina 2 HS Fe(III) dFe-O oxo 1.78 Å dFe-O 2-2.20 Å antiferromagnetic coupling (J=-71cm -1 )
- 22. Hemocianina deoxyHc: 2 Cu(I) Cu-Cu 3.7Å oxyHc: -peroxo Cu II 2 antiferromagnetic coupling (diamagnetic) Compuestos modelos O 2 his his his his his his
- 23. Modelos del sitio activo de hemocianina