PDF de transporte de materia
•
0 gefällt mir•148 views
El documento describe diferentes medidas de concentración, incluyendo concentración de masa (gramos por litro), concentración molar (moles de soluto por litro de disolución), fracción de masa (masa de soluto dividida por la masa total de la disolución) y fracción molar (moles de soluto divididos por los moles totales de la disolución). Todas estas medidas se utilizan para cuantificar la cantidad de soluto en una disolución.
Melden
Teilen
Melden
Teilen
Downloaden Sie, um offline zu lesen
Weitere ähnliche Inhalte
Ähnlich wie PDF de transporte de materia
Ähnlich wie PDF de transporte de materia (20)
Mehr von AnaGabrielaMiranda
Mehr von AnaGabrielaMiranda (20)
Fuentes alternativas de energia a los paneles solares

Fuentes alternativas de energia a los paneles solares
Kürzlich hochgeladen
Kürzlich hochgeladen (20)
Programacion Anual Matemática4 MPG 2024 Ccesa007.pdf

Programacion Anual Matemática4 MPG 2024 Ccesa007.pdf
Caja de herramientas de inteligencia artificial para la academia y la investi...

Caja de herramientas de inteligencia artificial para la academia y la investi...
Sesión de aprendizaje Planifica Textos argumentativo.docx

Sesión de aprendizaje Planifica Textos argumentativo.docx
La empresa sostenible: Principales Características, Barreras para su Avance y...

La empresa sostenible: Principales Características, Barreras para su Avance y...
Tema 8.- PROTECCION DE LOS SISTEMAS DE INFORMACIÓN.pdf

Tema 8.- PROTECCION DE LOS SISTEMAS DE INFORMACIÓN.pdf
SELECCIÓN DE LA MUESTRA Y MUESTREO EN INVESTIGACIÓN CUALITATIVA.pdf

SELECCIÓN DE LA MUESTRA Y MUESTREO EN INVESTIGACIÓN CUALITATIVA.pdf
AFICHE EL MANIERISMO HISTORIA DE LA ARQUITECTURA II

AFICHE EL MANIERISMO HISTORIA DE LA ARQUITECTURA II
Plan Refuerzo Escolar 2024 para estudiantes con necesidades de Aprendizaje en...

Plan Refuerzo Escolar 2024 para estudiantes con necesidades de Aprendizaje en...
proyecto de mayo inicial 5 añitos aprender es bueno para tu niño

proyecto de mayo inicial 5 añitos aprender es bueno para tu niño
LABERINTOS DE DISCIPLINAS DEL PENTATLÓN OLÍMPICO MODERNO. Por JAVIER SOLIS NO...

LABERINTOS DE DISCIPLINAS DEL PENTATLÓN OLÍMPICO MODERNO. Por JAVIER SOLIS NO...
PDF de transporte de materia
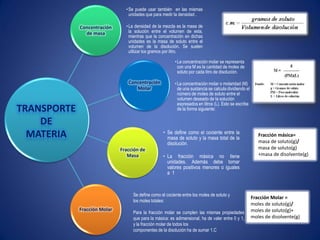
- 1. • Se puede usar también en las mismas unidades que para medir la densidad . Concentración de masa • La densidad de la mezcla es la masa de la solución entre el volumen de esta, mientras que la concentración en dichas unidades es la masa de soluto entre el volumen de la disolución. Se suelen utilizar los gramos por litro. • La concentración molar se representa con una M es la cantidad de moles de soluto por cada litro de disolución. Concentración Molar TRANSPORTE DE MATERIA • La concentración molar o molaridad (M) de una sustancia se calcula dividiendo el número de moles de soluto entre el volumen deseado de la solución expresados en litros (L). Esto se escribe de la forma siguiente: • Se define como el cociente entre la masa de soluto y la masa total de la disolución. Fracción de Masa • La fracción másica no tiene unidades. Además debe tomar valores positivos menores o iguales a 1 Se define como el cociente entre los moles de soluto y los moles totales: Fracción Molar Para la fracción molar se cumplen las mismas propiedades que para la másica: es adimensional, ha de valer entre 0 y 1, y la fracción molar de todos los componentes de la disolución ha de sumar 1.C Fracción másica= masa de soluto(g)/ masa de soluto(g) +masa de disolvente(g) Fracción Molar = moles de soluto(g)/ moles de soluto(g)+ moles de disolvente(g)