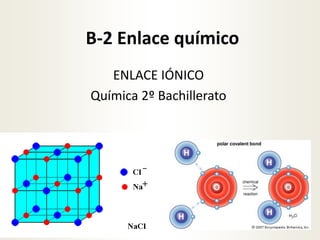
Enlace iónico. Química bachillerato
- 1. B-2 Enlace químico ENLACE IÓNICO Química 2º Bachillerato 1 Javier Valdés Colegio Inmaculada Gijón
- 2. Índice Introducción 1. ¿Por qué se unen los átomos? 2. Repaso Tipos de enlace Enlace iónico 1. Enlace Iónico y energía 2. Calculo de la Energía de red. Ciclo Born-Haber - Ejemplos PAU 3. Estructuras cristalinas - Factores de que dependen - Tipos de red - Ejemplos PAU 4. Propiedades de los compuestos iónicos
- 3. ¿Por qué se unen los átomos? • En la naturaleza siempre se busca el estado más estable • Los átomos se unen si así consiguen una situación de menor energía (más estable), que por separado • Para ello ponen en juego sus electrones más externos, electrones de valencia. Máxima estabilidad Mínima energía
- 4. Relación entre la distancia interatómica y la energía del sistema 4
- 5. Repaso Tipos de enlaces https://youtu.be/6-TarXU6ZKM Tipo de enlace Electrones Se da entre Concepto clave Estructura Ejemplos Iónico Ganancia y pérdida de electrones Entre iones Fuerzas electrostáticas Redes cristalinas NaCl, CaF2 Covalente Compartir pares de electrones entre dos átomos Entre átomos Átomos muy próximos para poder compartir electrones Moléculas independientes H2O, NH3, H2 Red covalente atómica SiO2, diamante, grafito Metálico Compartir electrones entre muchos átomos Entre átomos de metales Nube electrónica Red metálica Fe, Na, Zn…
- 7. Enlace iónico Metal • Baja energía de ionización • Pierde electrones con facilidad • Forma iones positivos No Metal • Alta Afinidad electrónica • Tiende a ganar electrones • Forma iones negativos Fuerzas de atracción electrostáticas
- 8. Enlace iónico y energía Planteamiento inicial El enlace se forma si se desprende energía Los productos son más estables que los átomos por separado Balance de energía negativo X (g) X– (g) Afinidad electrónica del no metal ( HAE <0) Me (g) Me+ (g) Energía de ionización del metal ( HEI >0) Estudiando las energía implicadas (a primera vista) en la formación del compuesto iónico: Aparentemente el compuesto iónico MeX se formará solo si: Energía de ionización del metal + Afinidad electrónica del no metal < 0 (Balance de energía negativo)
- 9. • Pero no siempre es así… • Y los compuestos se forman!!??? Caso del NaCl Enlace iónico y energía Cl (g) + e- Cl– (g) ( HAE = –348’8 kJ) Na (g) Na+ (g)+ e- ( HEI = +495’4 kJ) El NaCl se forma, y es estable, a pesar de que la AE del no metal no llega a compensar al EI del metal Debe haber más energías implicadas Energía de Red
- 10. Energía de red (reticular) Hret o U • El proceso por el que los iones se ordenan en los nudos de la red estabiliza el sistema: se desprende energía • Al ser una energía desprendida es <o • Permite explicar la formación del compuesto iónico en los casos en que AE del no metal no llega a compensar al EI del metal • No puede calcularse experimentalmente Es la energía desprendida en la formación de un compuesto iónico sólido a partir de sus iones en estado gaseoso
- 11. • No puede medirse experimentalmente • Método indirecto para calcularla: ciclo de Born y Haber • Consiste en calcular todas las energía del proceso de formación del compuesto iónico desde sus elementos en estado más estable, por dos vías e igualarlas… Energía de red (reticular) Hret o U Ley de Hess
- 12. Ciclo de Born y Haber • La reacción global de formación de NaCl es: Na (s) + ½ Cl2 (g) NaCl (s) (Hf = –411’1 kJ) • que puede considerarse suma de las siguientes reacciones: Na (s) Na (g) (Hsubl = +107’8 kJ) ½ Cl2 (g) Cl (g) (½ Hdis= +121’3 kJ) Cl (g) Cl– (g) (AHAE = –348’8 kJ) Na (g) Na+ (g) (AHEI = +495’4 kJ) Na+ (g) + Cl– (g) NaCl (s) (Hret = ?)
- 13. Ciclo de Born Haber
- 14. Ciclo de Born Haber
- 15. Ciclo de Born Haber
- 16. Ciclo de Born Haber (diagrama entálpico)
- 17. Ciclo de Born Haber (diagrama entálpico)
- 18. Ciclo de Born y Haber Na (s) Na (g) (Hsubl = +107’8 kJ) ½ Cl2 (g) Cl (g) (½ Hdis= +121’3 kJ) Cl (g) Cl– (g) (AHAE = –348’8 kJ) Na (g) Na+ (g) (AHEI = +495’4 kJ) Na+ (g) + Cl– (g) NaCl (s) (Hret = ?) • De donde puede deducirse que: Hret = Hf – (Hsubl + ½ Hdis + AHAE + AHEI) Hret = –411’1 kJ – (107’8 kJ + 121’3 kJ –348’8 kJ + 495’4 kJ) Na (s) + ½ Cl2 (g) NaCl (s) (Hf = –411’1 kJ) Hret = –786’8 kJ
- 20. Ejemplos PAU 2013 2012 Ver ejemplos resueltos en PAU temas
- 21. Estructura cristalina En los compuestos iónicos cada ion se rodea de iones de signo contrario ordenándose regularmente en el espacio: - Del modo más compacto posible - Minimizando las repulsiones - Red eléctricamente neutra - Estructuras tridimensionales que se repiten
- 22. Índice de coordinación: Es el número de iones de un signo que rodean a uno de signo contrario Estructura cristalina • El tamaño relativo de los iones • La carga de los iones. Electroneutralidad de la red (El cristal debe ser neutro, condiciona también la estequiometría) Factores de los que depende
- 23. Principales tipos de estructura cristalina • NaCl (cúbica centrada en las caras para ambos iones) – Índice de coord. para ambos iones = 6 • CsCl (cúbica para ambos iones) – Índice de coord. para ambos iones = 8 • CaF2 (cúbica centrada en las caras para el Ca2+ y tetraédrica para el F– ) – Índice de coord. para el F– = 4 – Índice de coord. para el Ca2+ = 8
- 25. Factores de los que depende Aumenta con la carga de los iones Ej: el CaO (Ca2+ y O2–) tiene Ered mayor que el NaCl (Na+ y Cl–). Disminuye con el tamaño de los iones Ej: El NaCl (Na+ y Cl–) tiene Ered mayor que el KBr Energía reticular (Es negativa, consideramos valores absolutos)
- 28. PREGUNTAS PAU
- 29. Propiedades de los compuestos iónicos • Puntos de fusión y ebullición elevados (tanto más cuanto mayor HU) Para fundirlos es necesario romper la red cristalina, estable por la cantidad de atracciones electrostáticas entre iones de distinto signo. • Son sólidos a temperatura ambiente. • Gran dureza • Solubilidad en disolventes polares e insolubilidad en disolventes apolares. • Conductividad en estado disuelto o fundido. Sin embargo, en estado sólido no conducen la electricidad. • Son frágiles
- 30. Disolución de un cristal iónico en un disolvente polar Solubilidad de un cristal iónico © Grupo ANAYA. Química 2º Bachillerato.
