Energía Libre, guía para biólogos, basada en la metodología POGIL
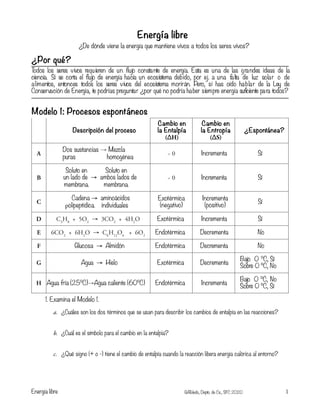
- 1. 1 A ~ 0 B ~ 0 C D C3 H8 + 5O2 → 3CO2 + 4H2 O E 6CO2 + 6H2 O → C6 H12 O6 + 6O2 F G H a. ¿Cuáles son los dos términos que se usan para describir los cambios de entalpía en las reacciones? 1. Examina el Modelo 1. b. ¿Cuál es el símbolo para el cambio en la entalpia? c. ¿Qué signo (+ o -) tiene el cambio de entalpía cuando la reacción libera energía calórica al entorno? ¿De dónde viene la energía que mantiene vivos a todos los seres vivos? ¿Por qué? Dos sustancias → Mezcla puras homogénea ¿Espontánea? Sí Sí Sí Sí No No Incrementa Incrementa Incrementa Decrementa Decrementa Decrementa Incrementa Energía libre Cambio en la Entalpía (∆H) Cambio en la Entropía (∆S) Modelo 1: Procesos espontáneos Descripción del proceso Exotérmica (negativo) Incrementa (positivo) Exotérmica Exotérmica Endotérmica Endotérmica Endotérmica Cadena → aminoácidos polipeptídica. individuales Soluto en Soluto en un lado de → ambos lados de membrana. membrana. Glucosa → Almidón Agua → Hielo Bajo 0 °C, Sí Sobre 0 °C, No Agua fría (25°C)→Agua caliente (60°C) Energía libre Todos los seres vivos requieren de un flujo constante de energía. Esta es una de las grandes ideas de la ciencia. Si se corta el flujo de energía hacia un ecosistema debido, por ej. a una falta de luz solar o de alimentos, entonces todos los seres vivos del ecosistema morirán. Pero, si has oído hablar de la Ley de Conservación de Energía, te podrías preguntar ¿por qué no podría haber siempre energía suficiente para todos? Bajo 0 °C, No Sobre 0 °C, Sí GAToledo, Depto. de Cs., SFC 2020
- 2. 2 POGIL™ 2. Consulta el Modelo 1. Para cada proceso descrito a continuación, indica si el cambio es endotérmico o exotérmico. b. Un cubo de hielo derritiéndose. ¡Lee esto! 4. Consulta el Modelo 1. a. ¿Cuál es el símbolo para el cambio en la entropía de un sistema? 6. Examina el Modelo 1. Para cada proceso descrito a continuación, indica si la entropía aumenta o disminuye. a. Colorante alimentario mezclado en agua. b. Una sustancia caliente se enfría a temperatura ambiente. c. La respiración de la glucosa y oxígeno para producir dióxido de carbono y agua. Actividades para biología a. Una planta que produce glucosa a partir de dióxido de carbono y agua, más energía lumínica. c. Aminoácidos formando una cadena polipeptídica. El cambio de energía neta para una reacción está relacionado con lo fuerte que son los enlaces y la cantidad que se rompen y forman durante la reacción. La rotura de enlaces requiere energía mientras que su formación libera energía. Si se forman más enlaces o estos son más fuertes que los rotos, la reacción será exergónica (se liberará energía neta). Si se rompen más enlaces o más enlaces fuertes se rompen de los que se forman, entonces la reacción será endergónica (se observará una absorción neta de energía). 3. De acuerdo con el Modelo 1, ¿todas las reacciones exotérmicas son espontáneas? Si no es así, proporciona un contra-ejemplo del Modelo 1. b. Cuando aumenta la entropía de un sistema, ¿qué signo se usa ( + o -)? 5. De acuerdo con el Modelo 1, ¿existe una correlación entre el cambio en la entalpía y el cambio en la entropía de un sistema? Si es así, describe la correlación.
- 3. 3 7. Para cada uno de los procesos descritos en el Modelo 1, decide en grupo si las moléculas en las sustancias tienen más orden (están más organizadas) antes o después de la reacción. Haz un círculo alrededor del lado de la reacción con más orden. 8. ¿Hay correlación entre el nivel de organización de las moléculas y un cambio en la entropía de acuerdo con los ejemplos dados en el Modelo 1? Justifica tu razonamiento. ¡Lee esto¡ La entropía de un sistema se puede considerar como una medida de la cantidad de desorden en las moléculas que forman el sistema. El estudio de la entropía se basa en la estadística. Solo hay unas pocas formas en las que un sistema puede organizarse y tener baja entropía; pero, en general, hay más formas en las que un sistema puede estar desorganizado y tener alta entropía. Por lo tanto, es más probable que los sistemas existan en los estados de mayor entropía. Piensa en tu dormitorio, si no gastaras energía para limpiarlo, ¿estará organizado o desorganizado? a. Agua de una acera mojada que se está evaporando b. Separación de una mezcla en las sustancias puras que la componen. c. Una planta que utiliza materias primas para formar una hoja en primavera. d. Hojas descomponiéndose en invierno. 10. ¿Es suficiente un aumento en la entropía de un sistema para hacer un proceso espontáneo? Justifica tu razonamiento con evidencia del Modelo 1. 9. Predice si los siguientes procesos tendrían un aumento o una disminución de la entropía sobre la base de lo que has aprendido del Modelo 1. Energía libre
- 4. 4 POGIL™ 11. Examina las reacciones exotérmicas del Modelo 1. Cuando ocurren esas reacciones, ¿qué sucede, típicamente, con la temperatura del entorno? 12. Predice el cambio en la entropía del entorno para una reacción exotérmica. Pista: En el modelo 1, busca y examina un sistema que haya cambiado la temperatura. 13. Predice el cambio en la entropía del entorno para una reacción endotérmica. 14. Escribe la letra en el paréntesis ( ) de al menos un proceso del Modelo 1 que ilustre cada una de las siguientes condiciones que resultarán en una reacción espontánea. )a. Tanto el sistema como el entorno tienen un aumento en la entropía. ( b. El aumento de la entropía del sistema supera la disminución de la entropía del entorno. ( ) c. El aumento de la entropía del entorno supera la disminución de la entropía del sistema. ( ) ¡Lee esto! (Ten en cuenta que el término "espontáneo" no implica que el cambio suceda rápidamente. La oxidación es espontánea en las condiciones adecuadas, pero aún puede ocurrir muy lentamente) Actividades para Biología Algunos de los procesos del Modelo 1 son espontáneos, es decir, ocurrirán sin que se realice ningún trabajo adicional en el sistema. Por ejemplo, un soluto difundirá a través de una membrana hasta que se igualen las concentraciones en ambos lados. Sin embargo, la glucosa no se forma espontáneamente en la atmósfera a partir del CO2 y H2O. La 2ª Ley de la Termodinámica establece que un proceso será espontáneo cuando se produzca un aumento de la entropía total en el universo, es decir, el sistema o el entorno deben tener un aumento en la entropía, o ambos.
- 5. 5 ∆G = ∆H – T∆S ¡Lee esto! 15. Consulta el proceso C del Modelo 1. a. El término ΔH en la ecuación de energía libre de Gibbs, ¿sería positivo o negativo? b. El término ΔS en la ecuación de energía libre de Gibbs, ¿sería positivo o negativo ? c. Explica cómo el cambio en la entalpía y la entropía del proceso C en el Modelo 1 resultaría en una 16. Usa la ecuación de energía libre de Gibbs para mostrar cómo el cambio en la entalpia y la entropía del proceso E del Modelo 1 no resultaría en una reacción espontánea. 17. Los procesos A y B en el Modelo 1 tienen cambios de energía muy mínimos. Explica por qué esos procesos son espontáneos reacción espontánea en todas las temperaturas. Energía libre Cuando un proceso es espontáneo se puede utilizar para hacer trabajo. Por ejemplo, la respiración de la glucosa se usa en organismos para ejecutar procesos celulares como la producción de enzimas. La cantidad de trabajo que se puede hacer mediante un proceso espontáneo se llama Energía Libre de Gibbs (lleva el nombre del matemático que desarrolló el concepto, en 1873). Josiah Willard Gibbs propuso la ecuación que los científicos utilizan ahora para calcular el cambio de energía libre para un proceso Cuando ΔG es negativo, el proceso es espontáneo y puede hacer trabajo (exergónico). Cuando ΔG es positivo, el proceso no es espontáneo. Debe realizarse trabajo en el sistema para que pueda proceder (endergónico). Nota que la temperatura en la ecuación está en Kelvin y siempre será un número positivo.
- 6. 6 18. Considera el proceso G en el Modelo 1. a. ¿Cuál es el cambio de entropía para el sistema? b. ¿Cuál es el cambio de entropía para el ambiente? ¡Lee esto! En los sistemas biológicos, los procesos exergónicos a menudo se combinan con otros endergónicos. Esto permite el gran grado de organización que vemos en los organismos. Los organismos no están violando la Segunda Ley de la Termodinámica. Más bien, están dejando una estela de desorden alrededor de ellos mientras comen, respiran y crecen. 19. Si alguna vez has estado acampando, es posible que hayas usado procesos acoplados para hacerte un poco de chocolate caliente por la noche. Agua calienteLeña + O2 CO2+ H2O Agua fría 20. Analiza el proceso aoplado de abajo. glucosa + O2 ATP ADP + FosfatoCO2+ H2O POGIL™ Actividades para Biología b. ¿Cuál de los procesos de arriba es endergónico y se ha hecho trabajo? a. ¿Cuál de los procesos de arriba es exergónico? a. ¿Cuál de los procesos de arriba es exergónico? c. ¿Qué factor debe ser mayor cuando la temperatura está por encima de 0°C (273 K), el cambio de entropía del sistema o el cambio de entropía del entorno? Explica tu razonamiento. b. ¿Cuál de los procesos de arriba es endergónico y se ha hecho trabajo?
- 7. 7 Preguntas de ampliación b. La tierra no es un sistema cerrado. En definitiva, ¿cuál es la fuente de toda la energía para la vida en la tierra? a. Explica por qué esto es verdad, basado en la Segunda ley de la termodinámica. 23. Piensa en un proceso donde el aumento de la entropía del sistema es exactamente igual a la disminución de la entropía del entorno. ¿Podría ser espontáneo ese proceso? Justifica tu raciocinio. 22. La vida no puede existir en un sistema cerrado (sin intercambio de materia ni de energía). 21. ¿Son sinónimo los términos exotérmico y exergónico? Justifica tu respuesta con ejemplos. Energía libre
