Pp tema4
- 2. Definiţie: Bazele sunt substanţe compuse în a căror moleculă intră un atom de metal şi un număr de grupări hidroxil (OH), egal cu valenţa metalului. Formula generală: Mn(OH)n Denumire: „hidroxid de „ + denumirea metalului + (valenţa lui)
- 3. - bazele solubile şi greu solubile sunt substanţe solide, cristalizate de culoare albă, se dizolvă în apă cu efect exoterm: NaOH, KOH, Ca(OH)2 bazele insolubile sunt substanţe solide, divers colorate: Cu(OH)2-albastru, Fe(OH)2- brun roşcat Soluţiile bazelor solubile sunt lunecoase la pipăit, cu aspect uleios şi au acţiune vătămătoare asupra organismului. Ele ard pielea, având efect caustic.
- 4. acţiunea asupra indicatorilor: - soluţia de turnesol(violet) - albastru - soluţia de fenolftaleină(incoloră) - roşu reacţia de neutralizare - acid + bază = sare + apă (definitie) reacţia bazelor solubile cu oxizi acizi: - bază + oxid nemetalic = sare + apă reacţia bazelor solubile cu săruri solubile: -bază solubilă + sare solubilă = bază insolubilă + altă sare
- 5. fabricarea săpunului şi a detergenţilor(NaOH, KOH); în construcţii – laptele de var sau varul stins: Ca(OH)2 reactivi chimici de laborator; industria coloranţilor; fabricarea unor medicamente; industria maselor plastice; industria celulozei şi hârtiei.
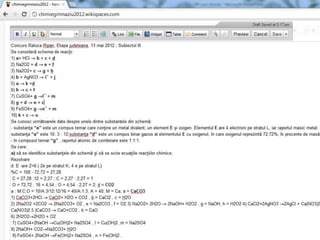
- 6. Experimentul Observaţii Ecuaţiile reacţiilor chimice Concluzii/ Utilizări 1.Acţiunea indicatorilor asupra bazelor solubile Turnesolul se colorează in albastru - Reacţii de recunoaştere a bazelor Fenolftaleină se colorează in roşu carmin - 2.Reacţia bazelor solubile cu oxizii acizi Apa de var limpede se tulbura Ca(OH)2 + CO2 → CaCO3 Recunoaşterea dioxidului de carbon 4.Reacţia bazelor cu acizii Soluţia roşu- carmin devine incoloră NaOH + HCl → NaCl + H2O Neutralizarea bazelor cu acizii Metoda de obţinere a unei sari. 4.Reacţia bazelor solubile cu unele săruri solubile Precipitat de culoare bruna FeCl3 + 3NaOH → Fe(OH)3↓+ 3NaCl Reacţii de obţinere a bazelor greu solubile Precipitat de culoare albastra CuSO4+ 2NaOH→Cu(OH)2↓+ Na2SO4