Quimica Trabajo V luis riera
•Als DOCX, PDF herunterladen•
0 gefällt mir•284 views
Quimica Trabajo V luis riera
Melden
Teilen
Melden
Teilen
Weitere ähnliche Inhalte
Was ist angesagt?
Was ist angesagt? (19)
Ähnlich wie Quimica Trabajo V luis riera
Ähnlich wie Quimica Trabajo V luis riera (20)
Trabajo práctico unidad v saia h 2015-ii victor goyo

Trabajo práctico unidad v saia h 2015-ii victor goyo
10 2-10-3 quimica- diana carolina burbano ruano guia no.4

10 2-10-3 quimica- diana carolina burbano ruano guia no.4
Kürzlich hochgeladen
Kürzlich hochgeladen (20)
c3.hu3.p1.p2.El ser humano y el sentido de su existencia.pptx

c3.hu3.p1.p2.El ser humano y el sentido de su existencia.pptx
Manejo del Dengue, generalidades, actualización marzo 2024 minsa

Manejo del Dengue, generalidades, actualización marzo 2024 minsa
5° SEM29 CRONOGRAMA PLANEACIÓN DOCENTE DARUKEL 23-24.pdf

5° SEM29 CRONOGRAMA PLANEACIÓN DOCENTE DARUKEL 23-24.pdf
Tarea 5_ Foro _Selección de herramientas digitales_Manuel.pdf

Tarea 5_ Foro _Selección de herramientas digitales_Manuel.pdf
Presentación de Estrategias de Enseñanza-Aprendizaje Virtual.pptx

Presentación de Estrategias de Enseñanza-Aprendizaje Virtual.pptx
libro para colorear de Peppa pig, ideal para educación inicial

libro para colorear de Peppa pig, ideal para educación inicial
Estas son las escuelas y colegios que tendrán modalidad no presencial este lu...

Estas son las escuelas y colegios que tendrán modalidad no presencial este lu...
PPT GESTIÓN ESCOLAR 2024 Comités y Compromisos.pptx

PPT GESTIÓN ESCOLAR 2024 Comités y Compromisos.pptx
TUTORIA II - CIRCULO DORADO UNIVERSIDAD CESAR VALLEJO

TUTORIA II - CIRCULO DORADO UNIVERSIDAD CESAR VALLEJO
Los Nueve Principios del Desempeño de la Sostenibilidad

Los Nueve Principios del Desempeño de la Sostenibilidad
Quimica Trabajo V luis riera
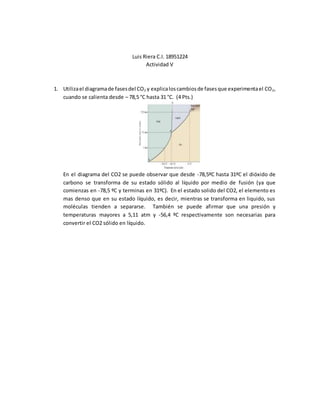
- 1. Luis Riera C.I. 18951224 Actividad V 1. Utilizael diagramade fasesdel CO2 y explicaloscambiosde fasesque experimentael CO2, cuando se calienta desde – 78,5 °C hasta 31 °C. (4 Pts.) En el diagrama del CO2 se puede observar que desde -78,5ºC hasta 31ºC el dióxido de carbono se transforma de su estado sólido al líquido por medio de fusión (ya que comienzas en -78,5 ºC y terminas en 31ºC). En el estado solido del CO2, el elemento es mas denso que en su estado líquido, es decir, mientras se transforma en liquido, sus moléculas tienden a separarse. También se puede afirmar que una presión y temperaturas mayores a 5,11 atm y -56,4 ºC respectivamente son necesarias para convertir el CO2 sólido en líquido.
- 2. 2-¿En qué volumenenlitrosde soluciónhayque disolver 230 gramos de HNO3 para que la presión osmótica a 225 ºC sea de 258,8 psi? (3 Pts.)
- 3. 3- A 50 ºC se tiene una mezcla formada por 61,26 gramos de naftaleno en 625 gramos de benceno. Calcular la presión de vapor de la solución en mmHg. Presión de vapor del benceno es 35,991 Kpa. (3 Pts.)
