Acetileno
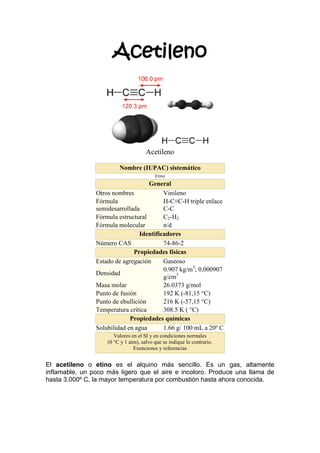
- 1. Acetileno Acetileno Nombre (IUPAC) sistemático Etino General Otros nombres Vinileno Fórmula H-C≡C-H triple enlace semidesarrollada C-C Fórmula estructural C2-H2 Fórmula molecular n/d Identificadores Número CAS 74-86-2 Propiedades físicas Estado de agregación Gaseoso 0.907 kg/m3; 0,000907 Densidad g/cm3 Masa molar 26.0373 g/mol Punto de fusión 192 K (-81,15 °C) Punto de ebullición 216 K (-57,15 °C) Temperatura crítica 308.5 K ( °C) Propiedades químicas Solubilidad en agua 1.66 g/ 100 mL a 20º C Valores en el SI y en condiciones normales (0 °C y 1 atm), salvo que se indique lo contrario. Exenciones y referencias El acetileno o etino es el alquino más sencillo. Es un gas, altamente inflamable, un poco más ligero que el aire e incoloro. Produce una llama de hasta 3.000º C, la mayor temperatura por combustión hasta ahora conocida.
- 2. Obtención del acetileno En petroquímica se obtiene el acetileno por quenching (el enfriamiento rápido) de una llama de gas natural o de fracciones volátiles del petróleo con aceites de elevado punto de ebullición. El gas es utilizado directamente en planta como producto de partida en síntesis; un proceso alternativo de síntesis, más apto para el laboratorio, es la reacción de agua con carburo cálcico (CaC2). Se forma hidróxido de calcio y acetileno. El gas formado en esta reacción a menudo tiene un olor característico a ajo debido a trazas de fosfina que se forman del fosfuro cálcico presente como impureza. aro primo Características El acetileno es un compuesto exotérmico. Esto significa que la descomposición en sus elementos libera calor. Por esto su generación suele necesitar elevadas temperaturas en alguna de sus etapas o el aporte de energía química de alguna otra manera. El acetileno es un gas explosivo si su contenido en aire está comprendido entre 2 y 82%. También explota si se comprime solo, sin disolver en otra sustancia, por lo que para almacenar se disuelve en acetona, un disolvente liquido que lo estabiliza. Usos del acetileno Primeros usos (s. XX) A principios del siglo XX, el acetileno tenía múltiples aplicaciones debido a la fijeza y claridad de su luz, su potencia calorífica su facilidad de obtención y su bajo costo. Los aparatos generadores se habían también perfeccionado siendo casi todos ellos del sistema en que el agua cae sobre el carburo estando la caída de aquélla graduada de tal modo por diversos juegos de válvulas, palancas y contrapesos que casi se llegó a evitar la sobreproducción de gas que tanto dañaba a los aparatos anteriores. El acetileno se utilizaba en generadores, en lámparas de minería o en el soplete oxiacetilénico empleado en la soldadura autógena produciendo temperaturas de hasta 3.000º, el alumbrado de proyectores para la marina y para cinematógrafos. Los automóviles llevaban también a principios del siglo en su mayoría faros con aparatos autogeneradores de acetileno. Se llegaron a construir diversos aparatos de salvamento como cinturones, chalecos, boyas, etc., en cuyo interior y en un depósito ad hoc llevaban una dosis de carburo de calcio dispuesto de tal suerte que al ponerse el carburo en contacto con el agua se produjera el gas acetileno dejando henchido convenientemente el aparato.[1] En la actualidad El acetileno se utilizaba como fuente de iluminación y de calor. En la vida diaria el acetileno es conocido como gas utilizado en equipos de soldadura debido a
- 3. las elevadas temperaturas (hasta 3.000 °C) que alcanzan las mezclas de acetileno y oxígeno en su combustión. El acetileno es además un producto de partida importante en la industria química. Hasta la segunda guerra mundial una buena parte de los procesos de síntesis se basaron en el acetileno. Hoy en día pierde cada vez más en importancia debido a los elevados costes energéticos de su generación. Disolventes como el tricloretileno, el tetracloretano, productos de base como viniléteres y vinilésteres y algunos carbociclos (síntesis según Reppe) se obtienen a partir del acetileno. Éste también se utiliza en especial en la fabricación del cloroetileno (cloruro de vinilo) para plásticos, del etanal (acetaldehido) y de los neoprenos del caucho sintético.
