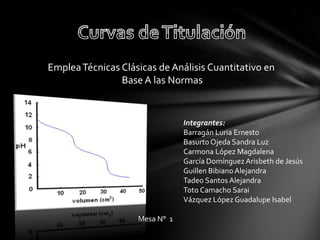
Curvas de titulación
- 1. Emplea Técnicas Clásicas de Análisis Cuantitativo en Base A las Normas Integrantes: Barragán Luria Ernesto Basurto Ojeda Sandra Luz Carmona López Magdalena García Domínguez Arisbeth de Jesús Guillen Bibiano Alejandra Tadeo Santos Alejandra Toto Camacho Sarai Vázquez López Guadalupe Isabel Mesa N° 1
- 2. El equilibrio acido-base es un tema muy importante dentro de la química, agricultura, la biología y la medicina. Equilibrio químico: cuando una reacción química de transformación ocurre al mismo ritmo que la transformación inversa, y por tanto no se producen cambios en la cantidad de cada compuesto Las titulaciones en donde se emplean ácidos y bases son muy utilizadas para el control analítico de muchos productos comerciales y la disociación de ácidos y bases ejerce una influencia importante en los procesos metabólicos de la célula viva. Es el mantenimiento de un nivel normal de la concentración de iones hidrogeno (H+) en los fluidos del organismo. El (H+) es un protón. La concentración de iones (H+) de una solución determina su grado de acidez. Bases son las que captan protones o sea aceptadoras de protones .
- 3. Neutra la que tiene una misma cantidad de iones hidrogeno y alcalinas. la curva de titulación es la gráfica que indica como el pH de la solución cambia durante el transcurso de la misma ( [*] el pH se gráfica contra el volumen de base o ácido agregado). Consiste en graficar el pH (o el pOH) contra mililitros de titulante. En solucion acuosa, los acidos y las bases fuertes se encuentran totalmente disocioados. El pH a lo largo de la titulacion se puede calcular directamente de las cantidades esqequiometricas de acido y base que van reaccionado. Se neutralizan cuando es un acido fuerte y una base fuerte. Por otra parte, cuando la reacción ocurre entre una base fuerte y un ácido débil, el anión del ácido sufre una hidrólisis, por lo que el pH al que ocurre la neutralización es mayor que 7. Y en la situación contraria, entre ácido fuerte y una base débil, el catión de la base sufre una hidrólisis produciéndose iones hidronio, por lo que el pH es menor que 7
- 4. Conceptos Una reacción de neutralización es una reacción entre un ácido y unas base, generalmente las reacciones acuosa acido base se produce agua y una sal. Por ejemplo: HCl (aq) + Na OH (aq) H2O (l) + Na Cl (aq) La titulación ácido-base es un procedimiento analítico cuyo objetivo es determinar la concentración de un analito con propiedades ácidas o básicas, utilizando una disolución valorada de una base o ácido, Las valoraciones ácido-base poseen las siguientes características • Se basan en una reacción volumétrica ácido-base. • El fundamento teórico de dicha reacción es la transferencia de protones entre el ácido y la base • El intervalo de viraje se caracteriza por un cambio brusco del pH. • Se necesita un indicador químico o un pH metro para monitorizar la valoración.
- 5. Los casos más frecuentes en las valoraciones ácido-base son: 1- Valoración de ácido fuerte con base fuerte 2- Valoración de base fuerte con ácido fuerte 3-Valoración de ácido débil con base fuerte 4-Valoración de base débil con ácido fuerte Durante la titulación, el punto en que se neutraliza un ácido o una base se denomina punto de equivalencia. Las curvas de titulación son las representaciones gráficas de la variación del pH durante el transcurso de la valoración. Dichas curvas nos permiten: Estudiar los diferentes casos de valoración (ácido fuerte vs. base fuerte; base fuerte vs. ácido fuerte; ácido débil vs. base fuerte; base débil vs. ácido fuerte). Determinar las zonas tamponantes y el pKa. Determinar el intervalo de viraje y el punto de equivalencia. Seleccionar el indicador ácido-base más adecuado.
- 6. Si se va añadiendo poco a poco una base a un ácido, el pH de la solución se incrementa con cada adición de base. El diagrama que representa la variación del pH durante la valoración se denomina curva de titulación. Si gráficamente el pH en función de la cantidad de base añadida, se observa una subida brusca en el punto de equivalencia. La región de subida brusca se llama punto final y se reconoce cuando el reactivo indicador cambia de color. El pH de la solución antes del punto de equivalencia se determina por la concentración del ácido que aún no ha sido neutralizado por la base. El pH en el punto de equivalencia es el pH de la sal resultante. Debido a que la sal que se produce por la reacción de un ácido fuerte y una base fuerte no se hidroliza, el punto de equivalencia se produce a pH 7,00. El pH de la solución después del punto de equivalencia está determinado por la concentración del exceso de base en la solución. Tipos de curvas: Sigmoidal segmento-linea
- 7. ^Titulación de un ácido fuerte con base fuerte Fase inicial: • Solución sólo contiene ácido fuerte. • El pH de la solución se determina usando la fórmula para determinar pH de un ácido fuerte. • La concentración de H es igual a la concentración del ácido fuerte. Fase antes del punto de equivalencia. • Se añade base pero no es suficiente para completar la reacción con el ácido. • El pH depende del ácido sin reaccionar. • H+] = moles sin reaccionar = moles H presentes - moles base añadidos V total V total
- 8. Punto de equivalencia. • La base añadida es justamente la necesaria para completar la reacción. • Los moles de ácido son igual a los moles de base. • El pH en esta etapa es igual a 7. Fase después del punto de equivalencia. • Hay exceso de base. • Se determina la concentración de OH- • [OH- ] = moles base exceso V total
- 9. Titulación de un ácido débil con una base fuerte Fase inicial • La solución contiene un ácido débil diluído. • El pH depende de la ionización del ácido. • Se usa la constante de equilibrio para buscar la concentración de H+ Fase antes del punto de equivalencia. • Se añade base, pero la reacción no llega acompletarse. • La solución contiene la sal que se ha formado en la reacción y el ácido que no ha reaccionado. Esta solución es un buffer. • El pH se determina usando la ecuación de Henderson-Hasselbach. • Base conjugada = moles añadidos/volumen total. • Acido = (moles ácido presente - moles base añadidos)/volumen total.
- 10. Punto de equivalencia • La base añadida es suficiente para completar la reacción. • La solución sólo contiene la sal formada que tiene el anión de un ácido débil. • Este anión reacciona con el agua liberandoiones OH, esta reacción determina el pH. • Se usa Kb Después del punto de equivalencia. • Hay exceso de base fuerte. • La solución contiene la sal formada hasta el punto de equivalencia y el exceso de base . • El pOH es determinado por los iones de OH de la base en exceso. • [OH] = (moles de base añadidos - moles de ácido que reaccionan)/volumen total
- 12. Cruvas de titulacion acido base tipicas: 50mlde acido monoprotico o.100M titulados con NaOH 0.100 Los valores de pKa para cada acido se muestra en las curvas
