ESQUEMA VACUNACIÓN MAYOR 5 AÑOS
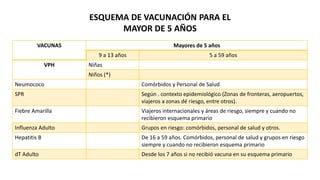
- 1. ESQUEMA DE VACUNACIÓN PARA EL MAYOR DE 5 AÑOS VACUNAS Mayores de 5 años 9 a 13 años 5 a 59 años VPH Niñas Niños (*) Neumococo Comórbidos y Personal de Salud SPR Según . contexto epidemiológico (Zonas de fronteras, aeropuertos, viajeros a zonas dé riesgo, entre otros). Fiebre Amarilla Viajeros internacionales y áreas de riesgo, siempre y cuando no recibieron esquema primario Influenza Adulto Grupos en riesgo: comórbidos, personal de salud y otros. Hepatitis B De 16 a 59 años. Comórbidos, personal de salud y grupos en riesgo siempre y cuando no recibieron esquema primario dT Adulto Desde los 7 años si no recibió vacuna en su esquema primario
- 2. VACUNA CONTRA dT ADULTO (Tétano y Difteria) TIPO DE VACUNA Inactivadas o muertas DESCRIPCIÓN Mezcla de toxoide tetánico y diftérico purificado y adsorbido en hidróxido o fosfato de aluminio. COMPOSICIÓN Una dosis de 0.5ml de vacuna contiene: Toxoide diftérico: < a 5 L.F (2 á 2UT) Toxoide tetánico: s a 5 L.F (2 a 40 UT) Absorbida: En fosfato dé aluminio al 1.25 mg Preservantes: 0.01% Tiomersal PRESENTACIÓN Frasco de 10 dosis de 5 ml. Suspensión blanca grisácea. Vacuna multidosis INDICACIONES Prevención de la difteria y tétanos. Cada 10 años se reforzará la inmunidad con una dosis de dT en personas qué recibieron esquema completo de Dt. DOSIS 0.5 ml. VIA Y SITIO DE ADMINISTRACION Vía intramuscular en la parte superior de la cara lateral externa del brazo, (región deltoides). V POSIBLES EFECTOS POST VACUNALES Dolor, eritema, induración en el sitio de la aplicación de la vacuna. MALESTAR GENERAL CONTRAINDICACIÓN Hipersensibilidad a cualquier componente de la vacuna en dosis previa. Reacciones neurológicas o reacciones alérgicas sistémicas posteriores a una dosis previa de dT. ESQUEMA DE VACUNACIÓN Varones ó mujeres ≥7 años de edad en adelante. Si no recibió la vacuna previamente: 1ra dosis al primer contacto con el servicio de salud. 2da dosis a los 2 meses de la primera 3ra dosis a los 6 meses de la primera dosis. Vacunación incompleta: No reiniciar. Completar con 1 o 2 dosis faltantes. Vacunación primaria completa: Refuerzo cada 10 años, a partir de la última dosis.
- 3. VACUNA CONTRA VIRUS PAPILOMA HUMANO (VPH) TIPO DE VACUNA Vacuna Recombinante DESCRIPCIÓN Protección contra la infección por los principales genotipos oncogénicos del virus del papiloma humano, asociados con el desarrollo del cáncer cervical y verrugas genitales. COMPOSICIÓN Una dosis de 0.5ml de vacuna contiene: 20 pg de VPH Proteína L1 tipo 6, 40 pg de VPH Proteína L1 tipo 11, 40 pg de VPH Proteína L1 tipo 16 y 20 pg de VPH Proteína L1 tipo 18. Sustrato levadura. Adyuvante: sulfato de hidroxifosfato de aluminio: 225 pg de aluminio amorfo PRESENTACIÓN Frasco monodosis de 0.5ml, líquido blanco. INDICACIONES Prevención de: Cáncer cervical causado por el VPH Tipo 16 y 18. Neoplasia Intraepitelial cervical (NIC) grado I y II. Verrugas genitales causadas por el VPH 6 y 11. DOSIS 0.5 ml. VIA Y SITIO DE ADMINISTRACION Vía intramuscular en la parte superior de la cara lateral externa del brazo, (región deltoides). POSIBLES EFECTOS POST VACUNALES Enrojecimiento, adormecimiento de la zona de inyección, alza térmica y sensación de fatiga. CONTRAINDICACIÓN Reacción alérgica grave (anafilaxia) con una dosis de vacuna ESQUEMA DE VACUNACIÓN Vacuna VPH Niñas Dos dosis: Niñas del 5to grado de primaria regular de Instituciones Educativas Públicas y Privadas y niñas que por alguna razón no estén estudiando que tengan de 9 a 13 años de edad. 1ra dosis: al primer contacto con el servicio de salud. 2da dosis: a los 6 meses de la Ira dosis A partir del 2023 se aplicará 1 sola dosis * Vacunas VPH Varones* Una dosis: Niños del 5to grado de primaria regular de II.EE. públicas y privadas y niños que por alguna razón no estén estudiando que tengan de 9 a 13 años de edad. 1ra dosis: al primer contacto con el servicio de salud. Incorporación de la vacuna VPH, para varones de 9 a 13 años en el año 2023.
- 4. TASA DE ESAVI LEVES ATRIBUIDOS A LA VACUNACIÓN O INMUNIZACIÓN Vacuna Reacción local tumefacción, enrojecimiento) Fiebre Irritabilidad, malestar y síntomas no específicos Antisarampionosa / SRP a hasta 10% hasta 5% hasta 5% VPH 25% a 84% 10% 1% a 7% Antineumocócica vacuna conjugada 10% a 20% 15% a 24% Influenza pandémica A(H1N1) 5% a 64% 1% a 11% 1% a 26% Hepatitis B hasta 30% en adultos hasta 5% en niñas y niños 1% a 6% poco frecuente TT/DT hasta 10% hasta 10% hasta 25%
- 5. TASA DE ESAVI SEVEROS ATRIBUIDOS A LA VACUNACIÓN Y TIEMPO DE APARICIÓN Vacuna EVENTO TIEMPO QUE TARDA EN APARECER TASAS POR 1 000 000 DE DOSIS Hepatitis B Anafilaxia 0 a 1 hora 1 a 2 VPH Anafilaxia 0 a 1 hora Rara Antineumocócica vacuna conjugada ninguna Influenza pandémica A(H1N1) Anafilaxia 0 a 1 hora < 2 Guillain-Barré 6 semanas 1 a 6 Síndrome óculo- respiratorio 90 a 466 Antisarampionosa Convulsiones febriles 7 a 12 días 17 a 50 TT/DT Neuritis del plexo braquial 2 a 28 días 5 a 10 Anafilaxia 0 a 1 hora 1 a 6 Absceso estéril 1 a 6 semanas 1 a 10
Notas del editor
- se puede administrar simultáneamente con cualquier otra vacuna virales, bacterianas u otras.
- se puede administrar simultáneamente con cualquier otra vacuna virales, bacterianas u otras.