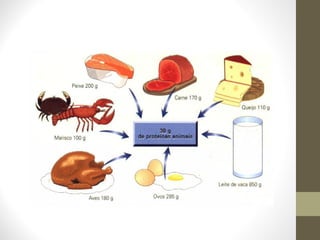
Funções das proteínas e seu metabolismo
- 1. PROTEÍNAS
- 2. FUNÇÃO DAS PROTEÍNAS •ANABÓLICA blocos formadores para todo material celular •CATABÓLICA combustível energético em certas condições proteínas musculares e hepáticas
- 3. CONJUNTO DE AMINOÁCIDOS PROTEÍNAS DA DIETA PROTEÍNAS TECIDUAIS SÍNTESE ANABOLISMO
- 4. Degradação de proteínas endógenas Proteínas intracelulares marcadas para degradação pela ligação com ubiquitina; Ubiquitina se liga proteínas para degradação; Complexo protéico proteossomo reconhece proteínas ligadas a ubiquitina e hidrolisam, liberando ubiquitina Livre; Proteínas são degradadas até aminoácidos e peptídeos.
- 6. DIGESTÃO E ABSORÇÃO inicia no estômago PEPSINA em meio ácido PROTEÍNA POLIPEPTÍDEOS Pepsina Ação mais importante digestão tripsina e quimotripsina ABSORÇÃO dipeptidases e aminotripeptidases jejuno e íleo transporte passivo não existe depósito de aminoácidos proteínas
- 11. AA em suas rotas catabólicas
- 12. Transferência de grupo amino de um aminoácido para outro; Aminoácidos desaminados por transaminação: Enzimas que catalisam a transaminação designadas aminotransferases ou transaminases, necessitam da coenzima piridoxal-fosfato (derivado vit B6). Transaminação
- 13. ALT AST
- 14. Desaminação Glutamato produzido por transaminação é desaminado, forma cetoglutarato libera amônia livre; Reações fígado e rins, fornecem α-cetoácidos e NH4, fonte de nitrogênio na síntese de uréia; Reação de transaminação e desaminação do glutamato rota onde grupos NH2 dos AA são liberados como NH4.
- 15. Desaminação pela glutamato desidrogenase
- 17. Metabolismo dos compostos nitrogenados •NH4 tóxica em altas concentrações; •Deve ser incorporada em compostos biologicamente utilizáveis; •A conversão de glutamato a glutamina é catalisada pela glutamina sintase na reação com gasto ATP; NH4 + glutamato + ATP glutamina + ADP + Pi
- 19. Ciclo de Cori
- 20. glutamato
- 24. Mutações podem levar a deficiências em enzimas que catalisam •Fenilcetonúria - •Dieta: restrição a fenilalanina •Albinismo - falta a enzima tirosinase, enzima responsável pela conversão de tirosina em melanina •Porfirias - faltam enzimas que catalisam reações de síntese de porfirinas; •Conseqüências neurológicas.
- 27. FENILCETONÚRIA
