Soluções Químicas e Cálculos de Concentração
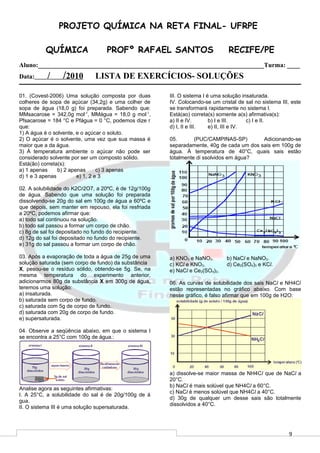
- 1. 9 PROJETO QUÍMICA NA RETA FINAL- UFRPE QUÍMICA PROFº RAFAEL SANTOS RECIFE/PE Aluno:______________________________________________________________________Turma: ____ Data: / /2010 LISTA DE EXERCÍCIOS- SOLUÇÕES 01. (Covest-2006) Uma solução composta por duas colheres de sopa de açúcar (34,2g) e uma colher de sopa de água (18,0 g) foi preparada. Sabendo que: MMsacarose = 342,0g mol-1 , MMágua = 18,0 g mol-1 , Pfsacarose = 184 °C e Pfágua = 0 °C, podemos dize r que: 1) A água é o solvente, e o açúcar o soluto. 2) O açúcar é o solvente, uma vez que sua massa é maior que a da água. 3) À temperatura ambiente o açúcar não pode ser considerado solvente por ser um composto sólido. Está(ão) correta(s): a) 1 apenas b) 2 apenas c) 3 apenas d) 1 e 3 apenas e) 1, 2 e 3 02. A solubilidade do K2Cr2O7, a 20ºC, é de 12g/100g de água. Sabendo que uma solução foi preparada dissolvendo-se 20g do sal em 100g de água a 60ºC e que depois, sem manter em repouso, ela foi resfriada a 20ºC, podemos afirmar que: a) todo sal continuou na solução. b) todo sal passou a formar um corpo de chão. c) 8g de sal foi depositado no fundo do recipiente. d) 12g do sal foi depositado no fundo do recipiente. e) 31g do sal passou a formar um corpo de chão. 03. Após a evaporação de toda a água de 25g de uma solução saturada (sem corpo de fundo) da substância X, pesou-se o resíduo sólido, obtendo-se 5g. Se, na mesma temperatura do experimento anterior, adicionarmos 80g da substância X em 300g de água, teremos uma solução: a) insaturada. b) saturada sem corpo de fundo. c) saturada com 5g de corpo de fundo. d) saturada com 20g de corpo de fundo. e) supersaturada. 04. Observe a seqüência abaixo, em que o sistema I se encontra a 25°C com 100g de água.: Analise agora as seguintes afirmativas: I. A 25°C, a solubilidade do sal é de 20g/100g de á gua. II. O sistema III é uma solução supersaturada. III. O sistema I é uma solução insaturada. IV. Colocando-se um cristal de sal no sistema III, este se transformará rapidamente no sistema I. Está(ao) correta(s) somente a(s) afirmativa(s): a) II e IV. b) I e III. c) I e II. d) I, II e III. e) II, III e IV. 05. (PUC/CAMPINAS-SP) Adicionando-se separadamente, 40g de cada um dos sais em 100g de água. À temperatura de 40°C, quais sais estão totalmente di ssolvidos em água? a) KNO3 e NaNO3. b) NaCl e NaNO3. c) KCl e KNO3. d) Ce2(SO4)3 e KCl. e) NaCl e Ce2(SO4)3. 06. As curvas de solubilidade dos sais NaCl e NH4Cl estão representadas no gráfico abaixo. Com base nesse gráfico, é falso afirmar que em 100g de H2O: a) dissolve-se maior massa de NH4Cl que de NaCl a 20°C. b) NaCl é mais solúvel que NH4Cl a 60°C. c) NaCl é menos solúvel que NH4Cl a 40°C. d) 30g de qualquer um desse sais são totalmente dissolvidos a 40°C.
- 2. 9 PROJETO QUÍMICA NA RETA FINAL- UFRPE QUÍMICA PROFº RAFAEL SANTOS RECIFE/PE e) a quantidade de NaCl dissolvida a 80°C é maior que 40°C. 07. (COVEST/02/2ª fase) A fenilalanina é um aminoácido utilizado como adoçante dietético. O gráfico abaixo representa a variação da solubilidade em água da fenilalanina com relação à temperatura. Determine o volume de água, em mililitros (mL), necessário para dissolver completamente 3,0 g da fenilalanina à temperatura de 40 °C. Considere que a densidade da água a 40 °C é 1,0 kg/L. 08. (Covest-98) O gráfico abaixo representa a variação de solubilidade em água, em função da temperatura, para algumas substâncias. Qual dessas substâncias libera maior quantidade de calor por mol quando é dissolvida? a) Na2SO4 b) Li2SO4 c) KI d) NaCl e) KNO3 09. (FUVEST-SP) Considere duas latas do mesmo refrigerante, uma versão “diet” e outra versão comum. Ambas contêm o mesmo volume de líquido (300 mL) e têm a mesma massa quando vazias. A composição do refrigerante é a mesma em ambas, exceto por uma diferença: a versão comum, contém certa quantidade de açúcar, enquanto a versão “diet” não contém açúcar (apenas massa desprezível de um adoçante artificial). Pesando-se duas latas fechadas do refrigerante, foram obtidos os seguintes resultados: Por esses dados, pode-se concluir que a concentração, em g/L, de açúcar no refrigerante comum é de, aproximadamente: a) 0,020g/L. b) 0,050g/L. c) 1,1g/L. d) 20g/L. e) 50g/L. 10. Um certo remédio contém 30g de um componente ativo X dissolvido num determinado volume de solvente, constituindo 150 mL de solução. Ao analisar o resultado do exame de laboratório de um paciente, o médico concluiu que o doente precisa de 3g do componente ativo X por dia, dividido em 3 doses, ou seja, de 8 em 8 horas. Que volume do medicamento deve ser ingerido pelo paciente a cada 8 horas para cumprir a determinação do médico? a) 50 mL. b) 100 mL. c) 5 mL. d) 10 mL. e) 12 mL. 11. Uma solução aquosa com concentração de 20g/litro apresenta: a) 20 g de soluto dissolvidos em 1 litro de água. b) 40 g de soluto dissolvidos em 0,5 litro de solução. c) 10 g de soluto dissolvidos em 0,5 litro de solução. d) 40 g de soluto dissolvidos em 4,0 litros de solução. e) 10 g de soluto dissolvidos em 2,0 litros de solução. 12. (Mackenzie – SP) Têm-se cinco recipientes contendo soluções aquosas de cloreto de sódio. É correto afirmar que: a) o recipiente 5 contém a solução menos concentrada b) o recipiente 1 contém a solução mais concentrada c) somente os recipientes 3 e 4 contêm soluções de igual concentração d) as cinco soluções têm a mesma concentração e) o recipiente 5 contém a solução mais concentrada 13. (UFRN-RN) Uma das potencialidades econômicas do Rio Grande do Norte é a produção de sal marinho. O cloreto de sódio é obtido a partir da água do mar nas salinas construídas nas proximidades do litoral.De modo geral, a água do mar percorre diversos tanques de cristalização até alcançar uma concentração determinada. Suponha que, numa das etapas do processo, um técnico retirou 3 amostras de 500 mL de um tanque de cristalização, realizou a evaporação com cada amostra e anotou a massade
- 3. 9 PROJETO QUÍMICA NA RETA FINAL- UFRPE QUÍMICA PROFº RAFAEL SANTOS RECIFE/PE sal resultante na tabela a seguir: A concentração média das amostras será de a) 48 g/L. b) 44 g/L. c) 42 g/L. d) 40 g/L. e) 50 g/L. 14. (Covest-2004) O rótulo de um frasco diz que ele contém uma solução 1,5 molar de NaI em água. Issoquer dizer que a solução contém: a) 1,5 mol de NaI / quilograma de solução. b) 1,5 mol de NaI / litro de solução. c) 1,5 mol de NaI / quilograma de água. d) 1,5 mol de NaI / litro de água. e) 1,5 mol de NaI / mol de água. 15. (UPE-2004-Q2) Analisando quantitativamente um sistema formado por soluções aquosas de cloreto de sódio, sulfato de sódio e fosfato de sódio, constatou-se a existência de: Baseado nos dados, pode-se concluir que a concentração de PO4 3– no sistema é: a) 0,525 mol/L. b) 0,12 mol/L. c) 0,36 mol/L. d) 0,24 mol/L. e) 0,04 mol/L. 16. A molaridade do íon Mg2+ e do (PO4)3- numa solução 0,4 molar de Mg3(PO4)2 é, respectivamente: a) 2 e 3. b) 3 e 2. c) 2,4 e 2,4. d) 0,4 e 0,4. e) 1,2 e 0,8. 17. (UFPE) Uma solução de um sulfato contém uma concentração 1,0 mol/L de íons sulfato (SO4 2– ). Podemos afirmar que esta solução pode conter: a) íons alumínio (Al3+ ) numa concentração 2/3 mol/L. b) íons férrico (Fe3+ ) numa concentração 1,0 mol/L. c) íons cloreto (Cl1– ) numa concentração 2,0 mol/L. d) íons nitrato (NO3 1– ) numa concentração 2/3 mol/L. e) íons bário (Ba2+ ) numa concentração 4/3 mol/L. 18. (COVEST/04/2ª fase) A água oxigenada ou peróxido de hidrogênio (H2O2), é vendida nas farmácias com concentrações em termos de “volumes”, que correspondem à relação entre o volume de gás O2, liberado após completa decomposição do H2O2, e o volume da solução aquosa. Sabendo que a equação química de decomposição da água oxigenada é H2O2(aq) H2O(g) + 1/2 O2(g), calcule a concentração molar de uma solução de água oxigenada de 24,4 volumes a 25°C e 1 atm. Dado: R = 0,082 atm x L / K x mol. 19. A concentração do cloreto de sódio na água do mar é, em média, de 2,95 g/L. Assim sendo, a molaridade desse sal na água do mar é aproximadamente: Dados: Na = 23 u.m.a.; Cl = 35,5 u.m.a. a) 0,050 mol/L. b) 0,295 mol/L. c) 2,950 mol/L. d) 5,000 mol/L. e) 5,850 mol/L. 20. A glicose, fórmula molecular C6H12O6, quando presente na urina, pode ter sua concentração determinada pela medida da intensidade da cor resultante da sua reação com um reagente específico, o ácido 3,5 - dinitrossalicílico, conforme ilustrado na figura: Imaginemos que uma amostra de urina, submetida ao tratamento mencionado, tenha apresentado uma intensidade de cor igual a 0,2 na escala do gráfico. É, então, correto afirmar que: Dado: Massa molar da glicose: 180g/mol. A quantidade de matéria (nº de mols) é dada por: n = m / M sendo m: massa; M = massa molar. a) a concentração de glicose corresponde a 7,5 g/L de urina. b) a amostra apresenta aproximadamente 0,028 mol de glicose por litro. c) a intensidade da cor, na figura, diminui com o aumento da concentração de glicose na amostra. d) a intensidade da cor da amostra não está relacionada com a concentração de glicose. e) a presença de glicose na urina é impossível, uma vez que ela não forma soluções aquosas. 21. Num refrigerante tipo “cola”, a análise química determinou uma concentração de ácido fosfórico igual a 0,245 g/L. a concentração de ácido fosfórico em mol/L, nesse refrigerante, é igual a: Dado: massa molar do ácido fosfórico = 98 g/mol. a) 0,0025 mol/L. b) 0,0050 mol/L. c) 0,025 mol/L. d) 0,050 mol/L. e) 0,250 mol/L. 22. Numa diluição de uma solução, podemos afirmar que: a) A massa do solvente permanece constante. b) A massa do soluto permanece constante.
- 4. 9 PROJETO QUÍMICA NA RETA FINAL- UFRPE QUÍMICA PROFº RAFAEL SANTOS RECIFE/PE c) O volume da solução permanece constante. d) A molaridade da solução permanece constante. e) A molalidade da solução permanece constante. 23. (Covest-91) Quantos mililitros de água devem ser adicionados a 400 mL de uma solução 3,00 mol/L de ácido nítrico para fornecer uma solução que é 2,0 mol/L deste ácido ? a) 100 mL. b) 200 mL. c) 300 mL. d) 400 mL. e) 500 mL. 24. (UNICAP-2007/Q2) 1 L de solução 0, 1M de Al2(SO4)3 foi preparada em laboratório e armazenada em um recipiente apropriado. Sobre a solução preparada pode-se afirmar que: 0 0 O número de mols do soluto, presente na solução, é igual a 2 (dois). 1 1 A solução contém mais de 33g de soluto. 2 2 Transferindo 25 mL da solução para um balão volumétrico de 250 mL e completando-se seu volume com água, a solução resultante fica quatro vezes mais diluída. 3 3 Separando a solução em dois recipientes, contendo quantidades iguais da mesma, cada nova solução terá uma concentração de soluto que vale metade da quantidade inicial. 4 4 Se o soluto Al2(SO4)3 apresentar-se 20% dissociado a concentração dos íons Al3+ será 0,04 M. 25. A partir do esquema de diluições representado a seguir, qual será a concentração no frasco D, após a execução das operações indicadas na seqüência de 1 a 5? a) 0,075 mol/L. b) 0,75 mol/L. c) 1,0 mol/L. d) 0,1 mol/L. e) 7,5 mol/L. 26. A respeito das soluções: 0 0 Quando diluímos uma solução, estamos aumentando o número de mol do soluto. 1 1 Quando diluímos uma solução, estamos aumentando o número de mol do solvente. 2 2 Na evaporação de uma solução aquosa de um composto iônico, o número de mols do soluto não se altera. 3 3 Quando misturamos duas soluções de mesmo soluto, porém com molaridades diferentes, a solução final apresenta uma molaridade com valor intermediário às molaridades iniciais. 4 4 Ao misturarmos soluções de solutos diferentes, sem que haja reação, na verdade o que ocorre é uma simples diluição de cada um dos solutos. 27. (COVEST/ 10) Um bom vinho apresenta uma graduação alcoólica de cerca de 13% (v/v). Levando- se em consideração que a densidade do etanol é 0,789 g mL-1 , a concentração de etanol, em mol L-1 , do vinho em questão, será (assinale o inteiro mais próximo): Dados: C = 12 g mol-1 , H = 1 g mol-1 e O = 16 g mol-1 . 28. (IME) Oleum, ou ácido sulfúrico fumegante, é obtido através da absorção do trióxido de enxofre por ácido sulfúrico. Ao se misturar oleum com água obtém- se ácido sulfúrico concentrado. Supondo que uma indústria tenha comprado 100Kg de oleum com conentração em peso de trióxido de enxofre de 20% e de ácido sulfúrico de 80%, calcule a quantidade de água que deve ser adicionada para que seja obitdo ácido sulfúrico com concentração de 95% em peso. Dados: Massas Atômicas (u.m.a): S= 32, O= 16 e H= 1. a) 42Kg b) 300Kg c) 100Kg d) 45Kg e) 104,5Kg 29. Julgue os itens: 0 0 A quantidade máxima de NaCl que se pode dissolver em 100g de água é de 36g, a 20°C. Nessa temperatura, foi preparada uma solução contendo 29,3g de NaCl em 100g de água. Podemos dizer que a solução preparada é uma solução saturada. 1 1 À temperatura ambiente, misturam-se 100mL de uma solução aquosa de MgSO4 de concentração 0,20mol/L com 50mL de uma solução aquosa do mesmo sal, porém, de concentração 0,40mol/L. A concentração (em relação ao MgSO4) da solução resultante será de 0,27 mol/L. 2 2 A hidrólise do DNA (ácido desoxiribonucléico) libera, entre outros compostos, ácido fosfórico, H3PO4. A quantidade desse ácido pode ser determinada por sua reação com NaOH, em
- 5. 9 PROJETO QUÍMICA NA RETA FINAL- UFRPE QUÍMICA PROFº RAFAEL SANTOS RECIFE/PE água: H3PO4 + 3 NaOH → Na3PO4 + 3 H2O Para isto, gastou-se 30 mL de solução aquosa 1,0 mol/L de NaOH. A quantidade de H3PO4 assim determinada é igual a 0,01 mol. 3 3 Na análise química de um suco de laranja, determinou-se uma concentração de ácido ascórbico (C6H8O6) igual a 264 mg/L. Nesse suco, a concentração de ácido ascórbico, em mol/L, é igual a 1,5×10-2 . 4 4 Tem-se 50 mL de solução 0,1 M de nitrato de Prata (AgNO3). Ao se adicionar 150 mL de água destilada à solução, esta passará a ter a concentração de 0,025 M. 30. Quando se misturam duas ou mais soluções de um mesmo soluto, a massa total de soluto na solução final será a soma das massas iniciais. Analogamente, o volume final será a soma dos volumes iniciais. Conseqüentemente, a concentração final C será: C=(m1+m2)/(V1+V2) Constante de Advogadro = 6,0 x 1023 0 0 A concentração molar da solução 01 é igual a 1 mol/L. 1 1 A concentração molar da solução 02 é igual a 6 mol/L. 2 2 Ao analisar a figura acima, conclui-se que a concentração da solução 03 é igual a 7 mol/L. 3 3 O número de moléculas de ácido fosfórico da solução 03 será de 2,4 x 1024 moléculas/L. 4 4 A massa de ácido fosfórico permanece constante durante o procedimento de mistura das duas soluções. 31. (UEMS-MS) A figura a seguir ilustra um equipamento bastante utilizado nos laboratórios de química. Com relação a esse equipamento é correto afirmar que: a) É usado na separação de compostos heterogêneos de sólidos e líquidos. b) É utilizado nos processos de separação de misturas heterogêneas de líquidos. c) É constituído de béquer e proveta. d) É usado para determinar a densidade de líquidos imiscíveis. e) É utilizado para realizar titulações. 32. (UPE-2009-Q2) A titulometria é utilizada comumente em laboratório, na análise química quantitativa. Em relação à análise titulométrica, é CORRETO afirmar que: a) após o término de uma titulação, o pH da solução resultante é igual a 7, quaisquer que sejam os titulantes e as amostras utilizadas. b) a solução usada como titulante, seja ela ácido forte ou base fraca, não pode ser incolor, pois, se assim o fosse, dificultaria a identificação do ponto de equilíbrio. c) tecnicamente é incorreto usar como titulante uma solução de ácido acético 0,001 mol/L, para titular uma solução de hidróxido de sódio concentrada. d) na titulação do ácido acetilsalicílico, utilizando-se como titulante o hidróxido de sódio, o pH no ponto de equivalência será menor que 7. e) a fenolftaleína é o indicador universal apropriado para a realização de todas as titulações, desde que a temperatura do laboratório não ultrapasse 20ºC. 33. Titulação é a operação que consiste em juntar lentamente uma solução a outra até o término da reação entre seus solutos, com a finalidade de determinar a concentração de uma das soluções a partir da concentração, já conhecida, da outra solução. Observe a figura abaixo: Considerando que foram gastos 100 mL de HNO3 para neutralizar 0,2 L de KOH, a concentração da solução de KOH, nessa análise, é: a) 0,5 mol/L b) 0,05 mol/L c) 0,1 mol/L d) 0,03 mol/L e) 0,02 mol/L 34. (UPE/SSA) O vinagre é uma solução aquosa diluída na
- 6. 9 PROJETO QUÍMICA NA RETA FINAL- UFRPE QUÍMICA PROFº RAFAEL SANTOS RECIFE/PE qual predomina o ácido acético, CH3COOH. Para determinar a percentagem massa/volume do referido ácido no vinagre, realiza-se uma titulação, utilizando- se uma solução padronizada de hidróxido de sódio 0,10 mol/L. Para isso, diluem-se 10,0mL de vinagre com água destilada em um balão volumétrico de 100,0 mL até a aferição. Foram gastos na titulação 5,0 mL do hidróxido utilizados como titulante, para titular uma alíquota de 10,0 mL da solução diluída. A percentagem massa/volume do vinagre analisado é Dados: ma(C) =12u, ma(O) =16u, ma( Na) = 23u, ma( H) = 1u A) 6% B) 2% C) 4% D) 5% E) 3% 35. (Covest-2009) O vinagre comercial contém ácido acético (CH3COOH). Na titulação de 6,0 mL de vinagre comercial com densidade 1,01 g mL-1 , gastaram-se 10,0 mL de uma solução 0,40 mol L-1 de hidróxido de sódio (NaOH). Qual é a porcentagem de ácido acético contido no vinagre analisado? (Dados: C = 12, H = 1 e O = 16). Anote o inteiro mais próximo. 36. Quando se adiciona uma solução de cloreto de cálcio a uma solução de carbonato de sódio forma-se uma solução de carbonato de cálcio insolúvel (utilizado como giz), de acordo com a equação: CaCl2 + Na2CO3 CaCO3 + 2 NaCl Para reagir completamente com 50 mL de solução 0,15 mol/L de Na2CO3, é necessário um volume de solução 0,25 mol/L de CaCl2 igual a: a) 15,0 mL. b) 25,0 mL. c) 30,0 mL. d) 50,0 mL. e) 75,5 mL. 36. (UPE/ 96) Preparou-se 100,00mL uma solução de um ácido diprótico de massa molar 162g/mol e densidade 1,80g/mL, diluindo-se 1,00mL deste ácido em quantidade suficiente de água destilada para completar o balão volumétrico até a aferição (100,00mL). Em seguida retira-se do balão 5,00mL da solução e titula-se com hidróxido de sódio 1N, gastando-se 1,00mL, para a completa neutralização. A pureza do ácido analisado é de: (H = 1u, S = 32u, O = 16u e Na = 23u) a) 70% b) 75% c) 83% d) 90% e) 78% 37. (UDESC-SC) Em um laboratório de química são colocados a reagir completamente 100 mL de solução de hidróxido de sódio com 30 mL de HCl 1,5 molar (mol/L). Pede-se: I - A molaridade da solução de hidróxido de sódio. II - A massa de hidróxido de sódio aí existente. A alternativa que apresenta corretamente o que se pede é: a) 0,225 mol/L e 1,8 g. b) 0,45 mol/L e 1,8 g. c) 0,045 mol/L e 1,8 g. d) 0,225 mol/L e 5,4 g. e) 0,45 mol/L e 3,6 g. 38. (IFAL/DOC/10) Um estudante deseja preparar em um balão volumétrico de 200 mL uma solução 0,2 mol/L de HCl. Para isso, este estudante dispõe de um frasco com 500 mL de ácido clorídrico concentrado com densidade de 1,18 g/mL e 36,5 % em massa. O volume retirado de ácido clorídrico concentrado do frasco de 500 mL e o volume de água destilada utilizada para o preparo dessa solução são, respectivamente: a) 12,01 mL e 187,99 mL. b) 4,38 mL e 195,62 mL. c) 33,40 mL e 166,60 mL. d) 3,39 mL e 196,61 mL. e) 3,18 mL e 196,82 mL. 39. (IFAL/DOC/10) Assinale a alternativa INCORRETA acerca de solubilidade e concentração das soluções: a) Se a atração soluto-solvente for mais forte que a atração solvente-solvente e soluto-soluto o processo de dissolução é exotérmico. b) O metanol é mais solúvel em água do que em dissulfeto de carbono. A explicação é que as forças entre moléculas de CH4O e CS2 são forças de dispersão e forças do tipo dipolo-dipolo induzido e com a água o CH4O pode formar ligações de hidrogênio. c) Sob pressão constante, a solubilidade de um gás num líquido diminui com a temperatura e se anula no ponto de ebulição. d) Para neutralizar 20 mL de uma solução 0,245 mol/L de H2SO4 são necessários, aproximadamente, 8 mL de solução 0,610 mol/L de NaOH. e) Uma solução de sacarose 0,1 mol/L é mais concentrada que uma solução de sacarose 3,42 g/L. 40. (IFPE/DOC/09) O hipoclorito de sodio e um sal vendido comercialmente em solucao aquosa com os nomes de agua sanitaria ou agua de lavadeira e possui efeito bactericida, sendo usado no tratamento de aguas. Assinale a alternativa abaixo que apresenta o numero de gotas de uma solucao de hipoclorito de sodio a 5 % (m/v) para deixar um litro de agua com 5 ppm do referido sal. Dados : volume de uma gota = 0,05 mL . Considerar volume final igual a 1 litro de solucao. a) 1 gota b) 2 gotas c) 3 gotas d) 4 gotase) 5 gotas 41. (IFPE/DOC/09) A vitamina C (acido ascorbico), esta presente em todas as frutas citricas, sendo a acerola a que apresenta maior teor. Uma das formas mais comuns de obtencao desta vitamina e atraves do suco de laranja, no entanto ao ser preparada, deve ser consumida o mais rapido possivel, pois a vitamina C perde sua acao em pouco tempo, em 68 minutos ela ja comeca a degradar. A vitamina C apresenta formula molecular C6H8O6, alem de ser acida, e tambem agente redutor. Uma das formas de se determinar o
- 7. 9 PROJETO QUÍMICA NA RETA FINAL- UFRPE QUÍMICA PROFº RAFAEL SANTOS RECIFE/PE teor de acido ascorbico num comprimido de vitamina C e titulando-se com iodo. Neste metodo, ocorrem duas reacoes: na reacao 1, e colocada uma solucao de iodo em excesso, para reagir com a vitamina C; em seguida, o excesso de iodo e titulado com solucao de tiossulfato de sodio (reacao 2). Admita que 80mL de solucao de I2(aq) 0,064 mol/L foram acrescentados a uma amostra de acido ascorbico. Depois da completa reacao, o iodo em excesso foi titulado com solucao de Na2S2O3 0,198 mol/L, consumindo 30,8 mL desta solucao ate o ponto de equivalencia. A massa, aproximada, de acido ascorbico na amostra, e em gramas igual a : (Dados: M(C) = 12g/mol, M(O) =16g/mol, M( H) = 1g/mol). a) 0,364g b) 0,512g c) 0,675g d) 0,275g e) 0,980 g. 42. (IFPE/DOC/09) Para se padronizar uma solucao em um laboratorio de quimica e essencial a utilizacao de padroes, os quais apresentam caracteristicas fundamentais para serem selecionados como padroes primarios, como por exemplo: são soluveis sob as condicoes de utilizacao, suas reacoes sao estequiometricas e praticamente instantaneas, sao de facil obtencao, entre outras. Assinale a alternativa que apresenta apenas substancias utilizadas como padrao primario em reacoes de acido-base. a) NaOH e HCℓ b) H4P2O7 e Mg2C2O4 c) K2Cr2O7 e HCℓO4 d) H2SO4 (concentrado) e LiOH e) KH(C8H4O4) e Na2B4O7 43. (IFPE/DOC/09) Deseja-se fazer a analise de um minerio de ferro em laboratorio. A uma amostra de 2,000g do minerio, acrescentase uma quantidade conveniente de uma solucao de acido cloridrico, e em seguida titula-se essa amostra com solucao de permanganato de potassio (KMnO4) 0,0190 mol/L, gastando-se 25,00mL desta solucao. A equacao ionica esta representada abaixo: Dado : M(Fe) = 56g/moL Assinale a alternativa que apresenta o percentual de ferro no minerio. a) 6,65% b) 12,90% c) 9,89% d) 21,06% e) 3,24% 44. (IFPE/DOC/09) Uma amostra solida, formada por Cloreto de bario e nitrato de potassio, pesando 600 mg e submetida a reacao com solucao de acido sulfurico diluido, em excesso, durante a adicao do acido, observou-se a formacao de um precipitado, filtrou-se o precipitado, que depois de lavado e seco pesou 0,050g. A solucao resultante da filtracao, acrescentou- se algumas gotas de H2SO4 diluido e nao houve mais formacao de precipitado. A solucao resultante foi transferida para um balao volumetrico de 250 mL e completou-se o volume com agua destilada ate afericao. Assinale a alternativa que indica o valor aproximado da concentracao de ions potassio (em ppm) na solucao resultante. Dados: massas molares em g/moL: Ba = 137; Cℓ = 35,5; S = 32; H = 1; O =16, K= 39; N =14 a) 222 ppm b) 345 ppm c) 309 ppm d) 277 ppm e) 858 ppm 45. (IFPE/DOC/09) Uma amostra de 20g de calcario foi colocada para reagir em um Becker contendo 500,0 mL de solucao de HCℓ 0,5 moL/L. O excesso deste acido foi titulado com solucao de hidroxido de bario 0,2 moL/L, gastando-se 40,0 mL desta solucao. (Dados: massas molares em g/moL: Ca = 40; C = 12; O = 16; H = 1; Cℓ = 35,5; Ba =137). Reacoes ocorridas. Indique a alternativa que corresponde ao percentual de carbonato de calcio na amostra original. a) 58,5% b) 34,7% c) 92% d) 45,5% e) 23,7% 46. (IFPE/DOC/09) O permanganato de potassio e um poderoso agente oxidante, utilizado na quimica analitca. Sua preparacao deve ser bastante cuidadosa. A solucao preparada deve ser armazenada em fraco ambar para evitar sua decomposicao devido a passagem da luz. O permanganato de potassio e dificil de ser obtido em condicoes de pureza elevada e completamente livre de dioxido de manganes. Em relacao a preparacao do permanganato de potassio, indique a alternativa correta. a) A titulacao de solucoes de permanganato de potassio, em meio acido, dispensa o uso de indicadores, ele funciona como um auto-indicador. Alem disso, o Mn2+ formado na reacao catalisa a sua decomposicao. b) Solucoes de permanganato de potassio, devem ser padronizadas com solucao padrao de acido sulfurico, apenas concentrado e a quente com temperatura em torno de 450C. c) Solucoes de permanganato de potassio tambem podem ser padronizadas com solucao de dicromato de potassio, desde que se utilize o meio fortemente alcalino.
- 8. 9 PROJETO QUÍMICA NA RETA FINAL- UFRPE QUÍMICA PROFº RAFAEL SANTOS RECIFE/PE d) Apos preparar uma solucao de permanganato de potassio e de fundamental importancia acrescentar um pouco de oxido de aluminio para evitar sua decomposição. e) Solucoes de permanganato de potassio sao muito utilizadas em laboratorios quimicos, para determinar o teor de peroxido de hidrogenio na agua oxigenada em meio fortemente basico. 47.(IFPE/DOC/09) Um laboratorista necessita preparar uma solucao de hidroxido de sodio 0,05 moL/L, no entanto nao dispoe desta base, mas dispoe de sodio metalico com 80% de pureza. Para resolver este problema, pesa-se uma aliquota de 5,75 g de sodio metalico, e coloca-se com bastante cuidado, utilizando a capela, em recipiente contendo 200mL de agua destilada. Apos o termino da reacao, filtra para retirar as impurezas e transfere para um balao volumetrico de 1000 mL, completando o volume com agua destilada ate a afericao. Indique a alternativa que mostra o volume necessario desta solucao, para preparar 500,0mL de solucao de hidroxido de sodio 0,05 moL/L. (Considere que as impurezas do sodio metalico sao insoluveis e nao reagem com a agua destilada). (Dados: Na = 23g/moL; H = 1g/moL e O = 16g/moL). a) 125 mL b) 220 mL c) 100 mL d) 158 mL e) 180 mL 48. (USP) 28 mL de uma solução 0,1 M de KMnO4 foram reduzidos em meio ácido por exatamente 22,50 mL de outra solução. Qual a normalidade da solução redutora? 49. (ITA) Calcular quantos mL de uma solução 0,2M de ácido sulfúrico são necessários para neutralizar 2g de hidróxido de magnésio. (Dados: H= 1u, O= 16u, Mg= 24u e S= 32,1u) 50. (ITA) Faz-se reagir 5 mL de ácido sulfúrico 0,1 M com NaOH. O ácido estará completamente neutralizado se forem empregados: a) 5 mL de NaOH 0,05 M b) 5 mL de NaOH 0,005 M c) 10 mL de NaOH 0,1 M d) 10 mL de NaOH 0,2 M e) 15ml de NaOH 0,2 M 51. (ITA) Dada a reação: 2KmnO4 + 5H2C2O4K2SO4 + 2MnSO4+ 8H2O +10 CO2 Quantos mL de H2C2O4 0,1 N reagem completamente com 50 mL de KmnO4 0,2M? a) 25 mL b) 100 mL c) 10 mL d) 5 mL e) nenhuma da respostas anteriores 52. (ITA) Adicionou-se um excesso de carbonato de amônio a 50 mL de uma solução de acetato de bário, tendo-se formando um precipitado de carbonato de bário de massa igual a 1,233 g. A molaridade da solução de acetato de bário era: (Dados: H= 1u, C= 12u, N= 14u e O=16u) a) 0,125 molar b) 0,0625 molar c) 0,0247 molar d) 0,00625 molar e) 0,00135 molar 53. (ITA) 9,3 g de óxido de sódio (Na2O) são despejados em 100 mL de ácido sulfúrico 2 M. Resultará daí: a) uma solução meutra b) uma solução ácida c) uma solução alcalina d) uma solução neutra e um precipitado e) nenhuma da respostas anteriores 54. (ITA) 0,2 mols de hidróxido de cálcio sólido são adicionados a 2 L de uma solução 0,4 M de ácido clorídrico. Depois da reação ter sido completada, a concentração de cárions hidrogênio, será: a) 0,5 M b) 0,1 M c) 0,2 M d) 0,3 M e) 0,4M 55. (ITA) Deseja-se preparar 100 mL de solução 0,1 formal (molar) de Na2S. Dispõ-se de solução 1 formal de NaHS e solução 0,25 formal de NaOH. Que volumes dessas duas soluções devem ser misturados e posteriormente levados a 1000 mL com água para obter a solução desejada? a) 100 mL de NaHS e 400 mL de NaOH b) 400 mL de NaHS e 100 mL e NaOH c) 300 mL de NaHS e 300 mL de NaOH d) 200 mL de NaHS e 200 mL de NaOH e) 333 mL de NaHS e 333 mL de NaOH f) nenhuma das repostas acima 56. (ITA) Deseja-se preparar 100 mL de solução 0,1M de Na2HPO4. Dispõ-se de NaOH 1M, H3PO4 1/3M e água. São necessários respectivamente os seguintes volumes: a) 30 mL de NaOH, 10 mL de H3PO4 e 60 mL de H2O b) 20 mL de NaOH, 40 mL de H3PO4 e 40 mL de H2O c) 20 mL de NaOH, 30 mL de H3PO4 e 50 mL de H2O d) 20 mL de NaOH, 10 mL de H3PO4 e 70 mL de H2O e) nenhuma das respotas anteriores. 57. (COVEST/2010.2) Se um frasco contendo uma solução aquosa de um reagente líquido possui em sua etiqueta as seguintes informações:
- 9. 9 PROJETO QUÍMICA NA RETA FINAL- UFRPE QUÍMICA PROFº RAFAEL SANTOS RECIFE/PE HCl concentrado (PM = 36,46 g/mol) d = 1,19 Kg/L T(título) = 37% em peso podemos afirmar que: A) a concentração desta solução em mol/L é dada por 1000xdxT/PM. B) a concentração desta solução em mol/L é dada por 10xdxT/PM. C) um kilograma desta solução contém 37 gramas de HCl. D) 36,46 g desta solução contêm 1 mol de HCl. E) um litro desta solução contém 1,19 Kg de HCl.
- 10. 9 PROJETO QUÍMICA NA RETA FINAL- UFRPE QUÍMICA PROFº RAFAEL SANTOS RECIFE/PE HCl concentrado (PM = 36,46 g/mol) d = 1,19 Kg/L T(título) = 37% em peso podemos afirmar que: A) a concentração desta solução em mol/L é dada por 1000xdxT/PM. B) a concentração desta solução em mol/L é dada por 10xdxT/PM. C) um kilograma desta solução contém 37 gramas de HCl. D) 36,46 g desta solução contêm 1 mol de HCl. E) um litro desta solução contém 1,19 Kg de HCl.
