El Agua
•
14 gefällt mir•3,016 views
La molécula de agua está formada por un átomo de oxígeno enlazado covalentemente a dos átomos de hidrógeno. Debido a la mayor electronegatividad del oxígeno, la molécula de agua tiene un extremo parcialmente positivo y otro parcialmente negativo, lo que le confiere polaridad. Esta polaridad permite que las moléculas de agua se atraigan entre sí mediante puentes de hidrógeno, dando lugar a propiedades extraordinarias como una alta capacidad calorífica y tensión superficial.
Melden
Teilen
Melden
Teilen
Empfohlen
Empfohlen
Weitere ähnliche Inhalte
Was ist angesagt?
Was ist angesagt? (20)
Proteinas de defensa, anticuerpos y gammaglobulinas 

Proteinas de defensa, anticuerpos y gammaglobulinas
Propiedades de las proteinas (laboratorio bioquimica)

Propiedades de las proteinas (laboratorio bioquimica)
Andere mochten auch
Andere mochten auch (20)
2. el atomo, isótopos, peso atómico y peso molecular

2. el atomo, isótopos, peso atómico y peso molecular
Ähnlich wie El Agua
Ähnlich wie El Agua (20)
Mehr von jegocon
Mehr von jegocon (20)
ImplementacióN Del Blog Educativo Como Herramienta PedagóGica

ImplementacióN Del Blog Educativo Como Herramienta PedagóGica
Kürzlich hochgeladen
Kürzlich hochgeladen (11)
PROYECTO FINAL. Tutorial para publicar en SlideShare.pptx

PROYECTO FINAL. Tutorial para publicar en SlideShare.pptx
Refrigerador_Inverter_Samsung_Curso_y_Manual_de_Servicio_Español.pdf

Refrigerador_Inverter_Samsung_Curso_y_Manual_de_Servicio_Español.pdf
How to use Redis with MuleSoft. A quick start presentation.

How to use Redis with MuleSoft. A quick start presentation.
EL CICLO PRÁCTICO DE UN MOTOR DE CUATRO TIEMPOS.pptx

EL CICLO PRÁCTICO DE UN MOTOR DE CUATRO TIEMPOS.pptx
Avances tecnológicos del siglo XXI y ejemplos de estos

Avances tecnológicos del siglo XXI y ejemplos de estos
Resistencia extrema al cobre por un consorcio bacteriano conformado por Sulfo...

Resistencia extrema al cobre por un consorcio bacteriano conformado por Sulfo...
El Agua
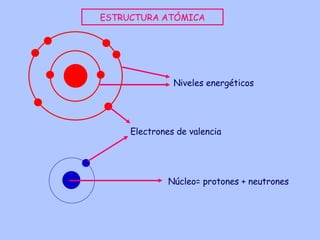
- 1. Núcleo= protones + neutrones Electrones de valencia Niveles energéticos ESTRUCTURA ATÓMICA
- 2. O H H Oxígeno Hidrógeno
- 3. Enlaces covalentes MOLÉCULA DE AGUA O H H
- 4. MOLÉCULA DE AGUA Mayor electronegatividad Menor electronegatividad O H H
- 5. MOLÉCULA DE AGUA Extremo parcialmente positivo Extremo parcialmente negativo O H H
- 6. Extremo positivo sobre átomos de hidrógeno, y extremo negativo sobre el átomo de oxígeno POLARIDAD DE LA MOLÉCULA DE AGUA DIPOLO
- 7. Al existir un dipolo en la molécula, ésta puede atraer a sus vecinas por fuerzas de atracción entre cargas de diferente signo. Estas fuerzas se denominan atracción dipolo-dipolo POLARIDAD DE LA MOLÉCULA DE AGUA
- 8. PUENTES DE HIDRÓGENO La atracción dipolo-dipolo, que es inusualmente fuerte, se denomina puente de hidrógeno
- 9. Enlaces covalentes La energía de los puentes de hidrógeno es aproximadamente un 1% del enlace covalente. La gran diferencia de energía distingue el enlace covalente, que es un enlace químico y por lo tanto muy fuerte, y el mal llamado enlace de hidrógeno, que sólo es una asociación física, porque es una atracción dipolo-dipolo.
- 10. ESTRUCTURA DE LA MOLÉCULA DEL AGUA Pares de electrones no enlazantes Pares de electrones enlazantes O 109,5º Mínima interacción de cargas negativas en el espacio TETRAEDRO REGULAR O H H - - + +
- 11. TETRAEDRO IRREGULAR Electrones más cerca de ambos núcleos Electrones ocupan más espacio alrededor del oxígeno ESTRUCTURA DE LA MOLÉCULA DEL AGUA 104,5º - - + +
- 12. Enlaces covalentes ESTRUCTURA DE LA MOLÉCULA DEL AGUA
- 13. EL AGUA 75% de la superficie de la tierra 65% a 95% de la masa de los seres vivos Surgió la vida Extraordinarias propiedades físicas y químicas
- 14. PROPIEDADES DEL AGUA Tensión superficial
- 15. PROPIEDADES DEL AGUA Capilaridad Movimiento ascendente de un líquido en un tubo estrecho fuerzas entre moléculas del líquido fuerzas entre las moléculas del líquido y el capilar atracción cohesiva
- 16. Fuerzas adhesivas (agua-vidrio) son mayores que cohesivas (agua-agua) menisco Agua Mercurio Fuerzas adhesivas (agua-vidrio) son menores que cohesivas (agua-agua) Capilaridad
- 17. Alto calor específico Cantidad de calor que necesita una sustancia para subir 1ºC la temperatura de 1 gramo de dicha sustancia Calor específico Gran parte del calor es usado para romper los puentes de hidrógeno Una vez conseguido esto, el calor se invierte en aumentar el movimiento de las moléculas, aumentando con ello la Tº se necesita mucho calor para que el agua aumente su temperatura no es fácil que el agua se caliente ni que se enfríe se desprende mucho calor cuando ésta se enfría
- 18. Congelación y Densidad grandes porciones flotantes de glaciares muy frecuentes en las regiones polares Icebergs En estado sólido (hielo), el agua es menos densa que en estado líquido
- 19. > 4ºC 0 - 4ºC Disminuye el movimiento Moléculas se acercan Moléculas se distancian Aumenta el volumen y por lo tanto disminuye la densidad Densidad = Masa Volumen
- 20. EL AGUA COMO DISOLVENTE Uniones ion-dipolo > Enlace iónico de la sal > Puentes de hidrógeno del agua De compuestos iónicos De compuestos polares Como Alcoholes Aldehidos Cetonas Establece puentes de hidrógeno con ellos
- 21. CICLO DEL AGUA Temperatura aumenta Temperatura disminuye
- 22. Se puede administrar calor sin cambiar su Tº Calor que rompe los enlaces que mantienen unidas a las moléculas, pero no aumenta su energía cinética
- 23. CICLO DEL AGUA