Processos de oxirredução
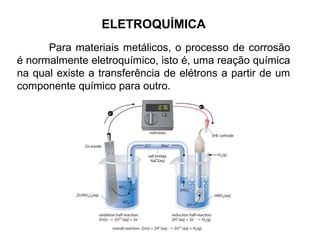
- 1. ELETROQUÍMICA Para materiais metálicos, o processo de corrosão é normalmente eletroquímico, isto é, uma reação química na qual existe a transferência de elétrons a partir de um componente químico para outro.
- 3. RREEAAÇÇÃÃOO DDEE OOXXIIRRRREEDDUUÇÇÃÃOO • REAÇÃO DE OXIRREDUÇÃO OU REDOX: Reação com transferência de elétrons de um reagente para outro, ou reação com variação de nox de pelo menos um elemento. • OXIDAÇÃO: Perda de elétrons ou aumento de nox. • REDUÇÃO: Ganho de elétrons ou diminuição de nox. • NÚMERO DE OXIDAÇÃO: É a carga elétrica dos átomos.
- 4. O agente oxidante em uma reação redox é a espécie que sofre redução. O agente redutor em uma reação redox é a espécie que sofre oxidação Fe (s) + Cu 2+ (aq) Fe 2+ (aq) + Cu (s) O átomo de Ferro metálico (Fe) perdeu dois elétrons, sofreu oxidação (Fe2+), provocou a redução do íon cobre (Cu2+) para cobre metálico (Cu), portanto é o AGENTE REDUTOR. O íon cobre (Cu2+) recebeu dois elétrons do átomo de Ferro metálico (Fe), sofreu redução (Cu), provocou a oxidação do Ferro metálico (Fe) para íon Ferro (Fe 2+), portanto é o AGENTE OXIDANTE.
- 5. Fe (s) + Cu 2+ (aq) Fe 2+ (aq) + Cu (s)
- 6. 2 Fe (s) + O2 (g) 2 FeO (s)
- 7. Células voltaicas • Usam a energia liberada em uma reação redox espontânea para realizar trabalho elétrico. • O elétrodo onde ocorre oxidação é chamado ânodo. • O elétrodo onde ocorre redução é chamado cátodo.
- 8. CONSIDERAÇÕES ELETROQUÍMICAS •Por exemplo, o metal Zn (zinco), que tem uma valência 2 (ou 2 elétrons de valência) pode experimentar oxidação de acordo com a reação: Zn (s) Zn +2 + 2e- •O material onde a oxidação ocorre é chamado de anodo
- 9. • Os elétrons gerados pelo metal que é oxidado devem ser transferidos para outro componente da qual fará parte, numa reação que é chamada reação de redução: 2 H+1 + 2e- H2 (g) • O componente onde ocorre a reação de redução é chamado de catodo.
- 10. • Uma reação eletroquímica global deve consistir de pelo menos uma reação de oxidação e uma reação de redução e oxidação e uma reação de redução e será a soma delas. Zn (s) Zn +2 + 2e- 2 H+1 + 2e- H2 (g) +____________________________________________________ Zn (s) + 2 H+1 Zn +2 + H2 (g)
- 13. PILHA
- 16. EFEITOS DO AMBIENTE As variáveis do ambiente de corrosão incluem velocidade de fluido, temperatura e composição, pode ter influência decisiva sobre as propriedades de corrosão dos materiais que estão em contato com esse ambiente.
- 17. FORMAS DE CORROSÃO Corrosão metálica é geralmente classificada em oito diferentes formas: •Uniforme; •Galvânica; •Em frestas; •Por pites ou localizada; •Intergranular; •Por lixíviação seletiva; •Erosão-corrosão; •Corrosão sob tensão.
- 18. Ataque Uniforme
