Modelos atómicos
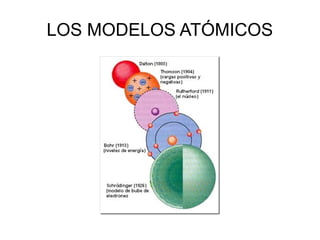
- 2. DISTINTOS MODELOS ATÓMICOS ● Dalton ● Thomson ● Rutherford ● Böhr
- 4. MODELO ATÓMICO DE DALTON Postulados: 1.La materia está formada por partículas muy pequeñas llamadas átomos, que son indivisibles y no se pueden destruir. 2.Los átomos de un mismo elemento son iguales entre sí, tienen la misma masa y propiedades. 3.Los átomos de diferentes elementos tienen masas diferentes. Comparando las masas de los elementos con los del hidrógeno tomado como la unidad propuso el concepto de peso atómico relativo. 4.Los átomos permanecen sin división, aun cuando se combinen en las reacciones químicas. 5.Los átomos, al combinarse para formar compuestos guardan relaciones simples. 6.Los átomos de elementos diferentes se pueden combinar en proporciones distintas y formar más de un compuesto. El modelo atómico de Dalton surgido en el contexto de la química, fue el primer modelo atómico con bases científicas, formulado entre 1803 y 1807 por John Dalton.
- 5. MODELO ATÓMICO DE THOMSON El modelo atómico de Thomson es una teoría sobre la estructura atómica propuesta en 1904 por Joseph John Thomson, quien descubrió el electrón, en 1898, mucho antes del descubrimiento del protón y del neutrón. 1.La materia es eléctricamente neutra, esto permitiría pensar que aparte de electrones, es posible que halla partículas con cargas positivas. 2.Es posible extraer electrones de los átomos, pero no del mismo modo las cargas positivas.
- 6. MODELO ATÓMICO DE BÖHR Postulados: El modelo atómico de Bohr o de Bohr- Rutherford es un modelo clásico del átomo, pero fue el primer modelo atómico en el que se introduce una cuantización a partir de ciertos postulados. El electrón solo podrá girar en ciertas órbitas circulares de energía y radios determinados, y al moverse en ellas el electrón no radiará energía. En ellas la energía del electrón será constante. En estas órbitas se cumplirá que el momento angular del electrón será múltiplo entero de h/2∏. Estas serán las únicas órbitas posibles. El electrón solo emitirá energía cuando estando en una de estas órbitas pase a otra de menor energía.